微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (17分)中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4?7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是: (填字母序号)。

②实验前,首先要准确配制一定物质的量浓度的酸性KMnO4溶液250mL,配制时需要的仪器除托盘天平、玻璃棒、烧杯、胶头滴管、量筒外,还需要 (填仪器名称)。
③该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol?L-1FeSO4、0.02mol?L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。
 物理量 物理量
实验序号
| V[0.10mol?L-1FeSO4]
/mL
|
|
| KMnO4溶液褪色所需时间t/s
|
1
| a
|
|
| t1
|
2
| a
|
|
| t2
(2)常温下,探究小组乙将0.1 mol・L-1盐酸滴入20 mL 0.1 mol・L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如右图所示。
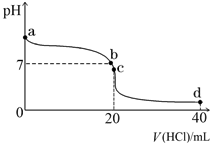
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)= 。
②b点处溶液中c (Cl-) c (NH4+)(填“>”、“<”或“=”)。
③取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释: 。
④d点所示溶液中离子浓度由大到小的排序是 。
2、选择题 将0.2 mol・L-1 HCN溶液和0.1 mol・L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系中正确的是
A.c(HCN) < c(CN―)
B.c(Na+)= c(CN―)
C.c(HCN)― c(CN―) = c(OH―)
D.c(HCN)+ c(CN―) =" 0.1" mol・L-1
3、填空题 工业制硫酸的过程中利用反应2SO2(g)+O2(g) 2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题: 2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
(1)一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1mol O2发生反应,则下列说法正确的是 。
A.若反应速率v (SO2)
4、选择题 下列说法正确的是( )
A.在Na2CO3、NaHCO3两溶液中,离子种类不相同
B.在等体积、等物质的量浓度的Na2CO3、NaHCO3两溶液中,阳离子总数相等
C.在NaHCO3和Na2CO3混合溶液中一定有:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
D.在NaHCO3和Na2CO3混合溶液中一定有:2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
5、填空题 (12分,每空2分)(1)常温下,将0.2 mol/L HCl溶液与0.2 mol/L氨水等体积混合(忽略混合后溶液体积的变化),测得混合后溶液的pH=6,试回答以下问题:
(1)混合后溶液呈酸性的原因是(用离子方程式回答) 。
(2)混合后溶液中由水电离出的c(OH-)为
(3)常温下,将0.2 mol・L-1的盐酸与 0.2mol・L-1的氨水混合,若所得的混合溶液中的pH=7,下列关系正确的是
A.[Cl-]>[NH4+]> [H+] > [OH-]
B.[NH4+]>[Cl-]>[OH-]>[H+]
C.[Cl-]=[NH4+]>[H+]=[OH-]
D.[NH4+]>[Cl-]>[H+]>[OH-]
(4)由电离常数可知酸性强弱: CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ②NaHCO3 ③Na2CO3
(5)将氯化铁溶液蒸干、灼烧,最后得到的固体是 。
(6)Cu(OH)2(s)  Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol?L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。 Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol?L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
|