��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Һ������Ũ�ȴ�С��ϵ�������
A��0.1 mol/L��NH4Cl��Һ�У�
B��0.1mol/L��CH3COONa��Һ�У�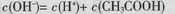
C��0.1 mol/LNa2S����Һ�У�
D��pH=2��������pH=12�İ�ˮ�������Ϻ�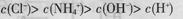
�ο��𰸣�D
���������
���������A���Ȼ����Һ��笠�����ˮ����Һ�����ԣ���Һ������Ũ�ȴ�СΪ��c��Cl-����c��NH4+����c��H+����c��OH-������ȷ��B��Ϊ��������Һ�������غ�ʽ����ȷ��C���κε������Һ�ж����������غ㣬���������غ��c��Na+��=2[c��S2-��+c��HS-��+c��H2S��]����C��ȷ��D��pH=12�İ�ˮ��pH=2��������Һ�У���ˮŨ�ȴ������ᣬ���ߵ������ϣ���ˮ��������Һ�ʼ��ԣ�����c��H+����c��OH-������ϵ���غ�֪c��Cl-����c��NH4+����D����
�����Ѷȣ�һ��
2������� �ơ�þ������ͭ���仯�����ڿ��к������������й㷺��Ӧ�á�
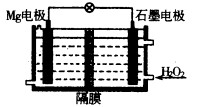
��1��Mg��H2O2��ؿ������������˼�ʻ��DZ�������õ���Ժ�ˮΪ�������Һ���ṹ��ͼ��ʾ����ع���ʱ�������ĵ缫��Ӧʽ ????????�������£��øõ�ص��200mL�ı�������ͭ��Һ(�缫Ϊ���Ե缫)����Ӧʱ��Һ��ˮ�ĵ���ƽ��??????�ƶ�(��������ҡ�����)��������24mg����Mg��������Һ��pH=?????(��������Һ������仯)��
��2�����õ�ⷨ������Ʒ�϶�ͭ���Է�ֹ������ʴ������˵����ȷ����????��
a�����ʱ��ͭ��ʯī��������������������ͭ�����������Һ
b����ƹ����У��¶����ߣ���ⷴӦ���ʼӿ�
c����ƹ����У�����ȫ��ת��Ϊ��ѧ��
d����ƹ����У�ͭ�����������ƶ���������ԭ��Ӧ
��3��NaHS����Ϊ��������ȥ��Һ�е�Cu2+�������£�NaHS��Һ�Լ��ԣ�ԭ����???????????????????(�����ӷ���ʽ�ͱ�Ҫ������˵��)������Cu2+�ķ�ˮ�м�������NaHS���壬��ˮ��Һ��pH??????(�������С�����䡱)��
�ο��𰸣���1��H2O2+2e��=2OH�������ң�2����2��ad����3
���������
�����������1�����⿼��ԭ���ԭ����Ӧ�á����ͻ�ѧ��Դ�����ԭ����Ӧ�á������װ��ͼ����Mg��H2O2����У�þ������������������Ӧ��H2O2��ʯī�缫�Ϸ�����ԭ��Ӧ�����������缫��ӦʽΪH2O2+2e��=2OH���������£��øõ�ص��200mL�ı�������ͭ��Һ(�缫Ϊ���Ե缫)��������ӦΪ:2H2O - 4e-== O2�� + 4H+����Ӧʱ��Һ��ˮ�ĵ���ƽ�������ƶ���������24mg����Mg��ת�Ƶĵ���Ϊ0.002mol�����ݵ����غ��������缫��Ӧʽ֪�����������������ʵ���Ϊ0.002mol��
�����Ѷȣ�һ��
3��ѡ���� ��һԪ��HA����Һ��һԪ��BOH����Һ�������ϣ���������Һ�����ԣ������й��ж���ȷ����
A�������ǰ�ᡢ�����ʵ���Ũ����ͬ����HA�϶�������
B����Һ��ˮ�ĵ���̶ȣ������Һ>��ˮ>BOH��Һ
C�������ǰ�ᡢ��pH֮�͵���14����HA�϶�������
D�������Һ������Ũ��һ�����㣺c(B+)>c(A��)>c(H+)>c(OH��)
�ο��𰸣�C
���������A�����ǡ�÷�Ӧ��ˮ���Լ��ԣ�����ȷ���������жϣ����Ĺ���������ѡ��B��һ����ȷ��C��ȷ����ʱ���ǹ����ģ���������ԡ����ݵ���غ��֪c(B+)��c(H+)��c(A��)��c(OH��)������ѡ��D�Dz����ܵģ���ѡC��
�����Ѷȣ�һ��
4��ѡ���� ��Na2HPO4��Һ�У�����������ƽ�⣺HPO42�� H++ PO43��?��HPO42-+H2O
H++ PO43��?��HPO42-+H2O H2PO4��+OH������֪����Һ�ʼ��ԡ���ʹ��Һ�е�HPO42����H+��PO43��Ũ�ȶ���С���ɲ�ȡ�ķ�����
H2PO4��+OH������֪����Һ�ʼ��ԡ���ʹ��Һ�е�HPO42����H+��PO43��Ũ�ȶ���С���ɲ�ȡ�ķ�����
A����ʯ��ˮ
B��������
C�����ռ�
D����ˮϡ��
�ο��𰸣�A
���������
�𰸣�A
A����Ca (OH)2ǰ��ƽ�������ƶ�������ƽ�������ƶ���B��������HPO42����H+Ũ�Ⱦ�����C��PO43�DŨ������D���ٽ�ˮ�⣬�����Լ�����H��Ũ������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��ȷ����(???)
A����̼������Һ����������������2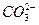 +H2O+SO2====2
+H2O+SO2====2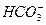 +
+
B��̼�������Һ�ĵ��뷽��ʽ��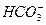
 H++
H++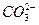
C������2 mol FeBr2����Һ��ͨ��1 mol������2Fe2++Cl2====2Fe3++2Cl-
D��NaHS��Һ��ˮ�⣺HS-+H2O H2S��+OH-
H2S��+OH-
�ο��𰸣�AC
���������B��̼�������Һ�ĵ��뷽��ʽ��д�ɣ�NH4HCO3===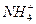 +
+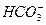 ��
�� �����Ѷȣ���
�����Ѷȣ���