微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图是制备和收集气体的实验装置,该装置可用于(?)
 ?
?
A.浓硝酸与铜反应制取二氧化氮
B.过氧化氢与二氧化锰反应制取氧气
C.浓氨水和生石灰反应制取氨气
D.浓盐酸和二氧化锰反应制取氯气
参考答案:B
本题解析:由装置图可以看出该反应不需要加热,生成的气体难溶于水,且不与水反应,所以只有选 项B正确。答案选B。
本题难度:一般
2、选择题 用下列两种方法制取氯气:①用含氯化氢146 g的浓盐酸与足量的二氧化锰反应 ②用87 g二氧化锰与足量的浓盐酸反应,则所得氯气
A.②比①多
B.①比②多
C.一样多
D.无法比较
参考答案:A
本题解析:
试题分析:浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,以此解答该题。反应的化学方程式为:4HCl(浓)+MnO2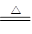 MnCl2+Cl2↑+2H2O,n(HCl)=146g÷36.5g/mol=4mol,浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,所以生成的n(Cl2)<1mol;
MnCl2+Cl2↑+2H2O,n(HCl)=146g÷36.5g/mol=4mol,浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,所以生成的n(Cl2)<1mol;
n(MnO2)=87g÷87g/mol=1mol,由于浓盐酸足量,生成的n(Cl2)=1mol,所以所得C12②比①多,答案选A。
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。明确随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应是答题的关键,有利于培养学生的逻辑推理能力。
本题难度:简单
3、选择题 下列实验不能达到预期目的的是
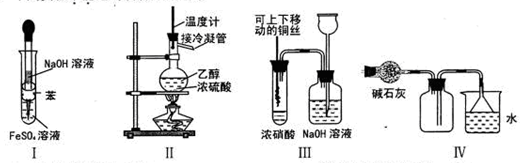
A.利用I制取Fe(OH)2
B.利用II装置制取CH2=CH2
C.利用III装置进行铜与浓硝酸反应的实验
D.利用IV装置收集NH3
参考答案:B
本题解析:
试题分析:苯不溶于水,密度比水小,则试管中溶液分层,位于上层的苯能隔绝空气,防止硫酸亚铁溶液氧化,将盛有NaOH溶液的长胶头滴管深入位于下层的硫酸亚铁溶液中,二者不仅能发生复分解反应,生成白色的氢氧化亚铁沉淀和硫酸钠溶液,而且能防止空气中的氧气将氢氧化亚铁氧化为氢氧化铁,故A项能达到实验目的;常温常压下乙醇是液体,在浓硫酸作用下,混合溶液加热到170℃时发生消去反应,生成乙烯,若混合溶液加热到140℃时发生取代反应,生成乙醚和水,因此温度计地水银球必须伸入乙醇和浓硫酸的混合液中,蒸馏时温度计水银球才能与蒸馏烧瓶支管口相平,故B项不能达到实验目的;浓硝酸与氢后金属铜接触时容易发生氧化还原反应,生成硝酸铜、二氧化氮和水,因此试管和集气瓶内出现红棕色气体,使铜丝离开液面时,反应停止,由于二氧化氮有毒,需要用NaOH溶液吸收多余的二氧化氮,二者发生氧化还原反应,生成硝酸钠、亚硝酸钠和水,空气沿长颈漏斗的长管进入集气瓶中,可以防止倒吸,故C项能达到实验目的;氨气是碱性气体,通常用碱性干燥剂除去其中混有的水分,氨气的密度比空气小,极易溶于水,因此不能排水法收集,只能用向下排空气法收集,图中氨气短进长出能干走集气瓶内的空气,多余氨气用水吸收时需要防止倒吸,倒扣漏斗的口与水面相平,既能充分吸收氨气,又能防止倒吸,故D错误。
本题难度:一般
4、填空题 下面是实验室可制取氨气的装置和选用的试剂,其中正确的是(???)
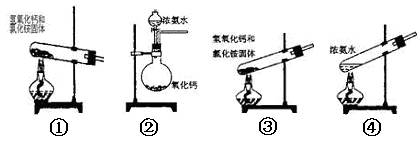
A.①③④
B.只有③
C.①②
D.①②④
参考答案:D
本题解析:①可以制取氨气;②在氨水中存在平衡:NH3+H2O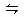 NH3・H2O
NH3・H2O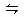 NH4++OH-,依据化学平衡移动原理,氧化钙与水反应放出大量热温度升高,使氨的溶解度减小而放出;氧化钙与水反应消耗水,促使氨放出;氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;③中试管口应略向下倾斜;④在氨水中存在平衡:NH3+H2O
NH4++OH-,依据化学平衡移动原理,氧化钙与水反应放出大量热温度升高,使氨的溶解度减小而放出;氧化钙与水反应消耗水,促使氨放出;氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;③中试管口应略向下倾斜;④在氨水中存在平衡:NH3+H2O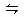 NH3・H2O
NH3・H2O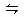 NH4++OH-,加热使温度升高,使氨的溶解度减小而放出。故正确的选项为D项。
NH4++OH-,加热使温度升高,使氨的溶解度减小而放出。故正确的选项为D项。
本题难度:简单
5、实验题 化合物KxFe(C2O4)y・3H2O(Fe为+3价)是一种光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。
Ⅰ.制备
 K2C2O4
K2C2O4
FeCl3
⑴结晶时应将溶液用冰水冷却并在黑暗处等待晶体的析出,这样操作的原因是:_________________
_______________________________________________。
⑵操作Ⅲ的名称是___________。
Ⅱ.组成测定
称取一定质量的晶体置于锥形瓶中,加入足量的蒸馏水和稀H2SO4,将C2O42-转化为H2C2O4后用0.1000 mol・L-1KMnO4溶液滴定,当消耗KMnO4溶液24.00mL时恰好完全反应;再向溶液中加入适量的还原剂,恰好将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液4.00mL。相关反应的化学方程式如下:
2 KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
⑶配制100mL 0.1000 mol・L-1KMnO4溶液及滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有_______________________________(填仪器名称)。两个滴定中,终点时溶液颜色为________色,且30 秒内不变色。
⑷该化合物KxFe(C2O4)y・3H2O中,x=_______。
参考答案:⑴用冰水冷却有利于析出更多的晶体,黑暗可以防止晶体分解
本题解析:本题涉及的制备是我们不熟悉的物质的制备,因此关于制备细节的考察,要么可以由我们以前的知识迁移而来,要么在题干中有所提示。
(1)故“冰水冷却”这句话很容易使我们想到是为了抑制溶解平衡,析出更多的晶体(这是知识的迁移);而“在黑暗处等待晶体析出”则和题干中的“光敏材料”对应,当推知黑暗是为了防止晶体见光分解。
(2)这是原有知识在新情境下的应用,考虑到前一步是结晶,结晶后自然要将晶体与母液分离、所以需要“过滤”, 如果再加上“洗涤”就更加严密。
(3)仍然是原有知识在具体新情境下的应用,题目中明确说道包含物质的量溶液配制和滴定实验,所以需要容量瓶和滴定管。关键是要准确写出“100mL容量瓶”,而KMnO4溶液有强氧化性,需用酸式滴定管盛放。关于终点颜色的判断,需要同学准确理解该滴定实验的原理,该实验是氧化还原滴定,终点时KMnO4溶液恰好过量一滴,故溶液会显紫红色。
(4)由题意求得:n(Fe3+)=0.001mol,n(C2O42-)=0.003mol,代入化学式,可求得x=3。
本题难度:一般