微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (4分)实验室用乙醇和浓H2SO4反应制取乙烯时,常发现反应混合液变黑,同时制得的乙醇具有刺激性气味,它是浓H2SO4氧化了乙醇的缘故。试求:
现有以下盛放于洗气瓶中的药品:
A.溴水
B.浓NaOH溶液
C.澄清石灰水
D.酸性KMnO4 E.品红溶液,请设计实验方案证明所制得的乙烯中混有CO2、SO2,同时乙烯能与溴水反应。
①写出气体通过洗气瓶时试剂放置的先后顺序(可重复选用)???????????????????。
②证明存在SO2的实验现象是??????????????????????????????????????????????;
③证明存在CO2的实验现象是????????????????????,
④证明C2H4与溴水反应的实验现象是???????????????????????????。
2、实验题 某研究小组在实验室中用铜粉(含铁粉5%以上)制取胆矾(CuSO4・5H2O)并检验其纯度,限选试剂:3 mol・L-1H2SO4溶液、浓硝酸、3%H2O2溶液、0.2 mol・L-1NaOH溶液、20% KSCN溶液、BaCl2溶液。有关物质溶解度如下表(单位g/100 g H2O):
温度/℃
| 0
| 20
| 40
| 60
| 80
| 100
|
CuSO4
| 14.3
| 20.7
| 28.5
| 40.0
| 55.0
| 75.4
|
Cu(NO3)2
| 81.8
| 124.8
| 163.1
| 181.8
| 207.8
| 247.3
?
(1)完成制取胆矾的实验方案。
实验步骤
| 预期现象
| 步骤1:除铁。将铜粉置于烧杯中,__________________
| _______________________
| 步骤2:溶解。将步骤1得到的铜粉置于烧杯中,
__________________________
| _______________________
| 步骤3:结晶。将步骤2所得溶液蒸发浓缩至液面有晶膜出现,冷却至室温,过滤得粗产品
| ?
?
(2)完成步骤1后,检验铜粉中的铁是否除尽的实验操作是___________。
(3)若胆矾中含有少量Cu(NO3)2・3H2O,测定其中CuSO4・5H2O的含量,实验步骤如下:称量胆矾样品的质量为m1,加水溶解,滴加足量BaCl2溶液,充分反应后过滤,将滤渣烘干、冷却,称得其质量为m2。样品中CuSO4・5H2O的质量分数为________(列出算式)。
3、填空题 (12分)过氧化氢是一种重要的化学产品,在工农业生产和日常生活中有着广泛应用,工业采用烷基薏醌法生产

根据生产过氧化氢原理和工艺,回答下列问题:
(1)该生产过氧化氢的原理中,原子利用率为??????????????。
(2)该工艺中有机溶剂为液态烷烃和酯类,能否用乙醇代替??????????
(3)为了提高经济效益,该工艺氢化反应,除了加催化剂外,还可采取的措施是??????。
A.适当加热???? B.加压?????????????????? C.增大工作液中有机溶剂的量
(4)该工艺中“后处理”的目的是?????????????????。
(5)该工艺中由35%的H2O2得到70%的H2O2可采取操作方法是?????????。
(6)硫酸酸化的过氧化氢溶液可溶解金属铜,试写出该反应的离子方程式为?????????。
4、填空题 (1)洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体:

①H2、②Cl2、③CH4、④HCl、⑤NH3、⑥CO2、⑦O2、⑧SO2、⑨C2H4
(A)若烧瓶是干燥的,把装置颠倒放置由B口进气,可收集的气体有_______
(B)若在烧瓶内充满水,可收集的气体有________,气体应由____口进入
(2)下列实验能达到实验目的且符合安全要求的是????????。
5、选择题 CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是(?)
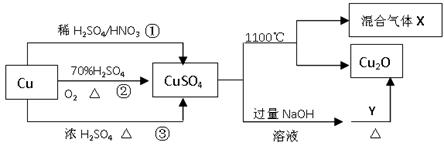
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1molCuSO4在1100℃所得混合气体X中O2一定为0.75mol
D.Y可以是葡萄糖
|
|