��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��֪25�桢101 kPa�£�ϡ��ǿ����ǿ����Һ��Ӧ���к���Ϊ57.3 kJ/mol��
��1��д����ʾϡ������ϡ�ռ���Һ������Ӧ���к��ȵ��Ȼ�ѧ����ʽ�� ��
��2��ѧ������ϡ������ϡ�ռ���Һ�ⶨ�к���װ����ͼ��
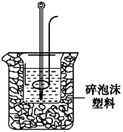
��ʵ��ʱ����IJ����������ձ�����Ͳ��裺 ��
�ڸ�װ������һ�������ǣ� 91Exam.org; ������øô���װ�òⶨ������� ���ƫ
�ߡ���ƫ�͡�����Ӱ�족��
�������������50 mL 0.25 mol/L��ϡ������50 mL 0.55 mol/L��ϡ�ռ���Һ�������Լ�����������
���ǣ� ���ڸ�ʵ������Ҫ�ⶨij�����ݣ�
���һ��ʵ�飬��Ҫ�ⶨ�����ݵĴ���Ϊ �Ρ�
��3��ѧ������2 mol/L���������ⶨ��п����п�۷�Ӧ�Ŀ����������ͼ����װ�ã�
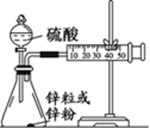
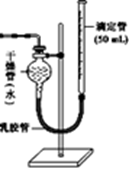
ͼ�� ͼ��
�ٸ�������ʵ��ⶨʱ����趨Ϊ10 min����ô����Ҫ�ⶨ����һ�������ǣ�
��
�������ͼ��װ���е������ռ�װ�ø�Ϊͼ��ʵ����ϴ���ȴ��������ȡ�ζ�����Һ�������Ŀ̶��������ֵζ�����Һ����ڸ������Һ�棬Ӧ�Ȳ�ȡ�IJ����ǣ� ���۸�ʵ�����У���������ᷴӦ�Ͽ���� ��
�ο��𰸣���1�� 1/2H2SO4(aq)��NaOH(aq)��1/2N
���������
�����������1���к�������һ�������£�ϡ��Һ�У�ǿ���ǿ�Ӧ����1molˮʱ���ų������������Ը÷�Ӧ���Ȼ�ѧ����ʽ��1/2H2SO4(aq)��NaOH(aq)��1/2Na2SO4(aq)��H2O ��H����57.3 kJ/mol����2����������Ҫ������Һ���¶��Լ���Ӧ����Ҫ���裬���Ի�ȱ�ٵIJ����������¶ȼơ����β�����������ڸ���װ��ͼ��֪ʵ����û����Ӳֽ�壨�����ϰ壩��ס�ձ��������ͻᵼ����������ʧ��ʵ��ⶨ�����ƫ�͡����������ƹ������Ա�֤������ȫ��Ӧ���Ӷ�����ʵ����ʵ������Ҫ��������������Һ���¶ȣ����������Ҫ����3�Σ�����Ӧǰ��ͼ����Һ�¶ȣ��Լ���Ӧ����Һ���¶ȡ���3����Ҫ�ȽϷ�Ӧ���ʵĴ�С�����˲���ʱ���⣬����Ҫ�ⶨ��ͬ��������������������������������������¶Ⱥ�ѹǿ��Ӱ�죬���Ա��뱣֤�����ѹǿ�ʹ���ѹ����ͬ�ģ������ȷ�IJ����������ƶ��ζ��ܣ�ֱ������Һ����ƽ��������п�۵ı������Ӧ���ʿ죬����Ӧ���ʽϿ����п�ۡ�
���㣺�Ȼ�ѧ����ʽ����д���к��ȵIJⶨ�Լ�Ӱ�췴Ӧ���ʵ�����
�����Ѷȣ�����
2��ѡ���� ����ͼ�������ȷ���ǣ� ��
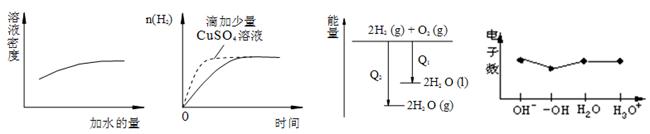
A��Ũ�����ϡ�͵�����п�۷�Ӧ
B�������������������仯
C��������������Ӧ�е�
D����������
�ο��𰸣�D
���������
���������A��������Һ���ܶ���Ũ�ȵ����������ͼ���ϣ�A����B��п������ͭ��Һ�����û���Ӧ��ͭ������п��Ȼ��пͭ����ԭ��ؼӿ췴Ӧ���ʣ�������������п�õ����������٣�ͼ�����B����C������ȼ������Һ̬ˮ�ų�����������������̬ˮ�ų���������ͼ�����C����D���������ĵ������ֱ���10��9��10��10��ͼ����ȷ��D��ȷ����ѡD��
���㣺���黯ѧͼ��ķ����ж�
�����Ѷȣ�һ��
3��ѡ���� ���л����������л�ѧ�����ǹ��ۼ����ǣ�������
A��Na2O2
B��NaOH
C��H2S04
D��BaCl2
�ο��𰸣�A�����������������Ӻ��������Ӽ�������Ӽ�����ԭ�Ӻ���ԭ��
���������
�����Ѷȣ���
4��ѡ���� ��20mL?Na2SO4��Һ�мӹ������Ȼ�����Һ���õ�2.33g������ԭ��Һ��Na+�����ʵ���Ũ��Ϊ
A.1.0mol/L
B.2.0mol/L
C.0.50mol/L
D.0.025mol/L
�ο��𰸣�A
���������������Na2SO4��Һ�мӹ������Ȼ�����Һ����SO42-+Ba2+�TBaSO4����2.33g����Ϊ���ᱵ���������ӷ���ʽ�ɼ�����������ӵ����ʵ����������û�ѧʽ���ж�Na+�����ʵ�����Ȼ�������Ũ�ȣ�
����Ȼ�����Һ��������2.33g����Ϊ���ᱵ�������������ʵ���Ϊ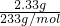 =0.01mol��
=0.01mol��
��Na2SO4�����ʵ���Ϊx����
SO42-+Ba2+�TBaSO4����
?1?????????? 1
?x?????????? 0.01mol
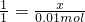 �����x=0.01mol��
�����x=0.01mol��
��Na+�����ʵ���Ϊ0.1mol��2=0.02mol��
ԭ��Һ��Na+�����ʵ���Ũ��Ϊ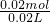 =1.0mol/L��
=1.0mol/L��
��ѡA��
���������⿼��ѧ���������ӷ�Ӧ����ʽ�ļ��㣬��ȷ��������Ϊ���ᱵ�������������ӷ�Ӧ�ɼ�����������ӵ����ʵ����ǽ����Ĺؼ���
�����Ѷȣ�����
5��ѡ���� 25�桢101 kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A��2H2(g)+O2(g) ="=" 2H2O��1����H��
�ο��𰸣�
���������
�����Ѷȣ�һ��