微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是 [???? ]
A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化碳气体
D.向水中加入食盐晶体
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列有关水的叙述正确的是 [???? ]
A.水是一种非电解质
B.纯水中c(H+)随着温度的升高而降低
C.由液态水结成冰的过程是一个熵增的过程
D.25℃,pH相同的氢氧化钠溶液与醋酸钠溶液,水的电离度前者小于后者
参考答案:D
本题解析:
本题难度:一般
3、实验题 某学生用0.200 0 mol・L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号) ,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) 。
(2)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟内不变色。
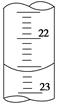
(3)如图是某次滴定时的滴定管中的液面,其读数为 mL。
(4)根据下列数据:请计算待测盐酸溶液的浓度为 mol/L
滴定次数
| 待测液体积(mL)
| 标准NaOH溶液读数记录(mL)
|
滴定前读数
| 滴定后读数
|
第一次
| 20.00
| 0.40
| 20.40
|
第二次
| 20.00
| 4.00
| 24.00
|
第三次
| 20.00
| 2.00
| 24.10
参考答案:(1)① 偏大
(2)无 粉红
(3)22.60
本题解析:(1)①用蒸馏水洗涤碱式滴定管后,不能立即注入NaOH溶液,应先用NaOH溶液润洗;否则所用NaOH溶液的体积偏大,导致测定盐酸的浓度偏大。(2)酚酞试剂在酸性溶液中呈无色,当溶液呈弱碱性时,溶液呈粉红色。(4)取前两次所 用NaOH溶液体积的平均值(第三次误差较大,舍去),然后代入公式进行计算:c(酸)V(酸)=c(碱)V(碱),故c(酸)=c(碱)V(碱)/V(酸)。
本题难度:一般
4、填空题 双氧水(H2O2)和水都是极弱电解质,但H2O2比水更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:______________________
(2)鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可以形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:______________________________
(3)水电离生成H3O+ 和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离方程式为:________________________________
参考答案:(1)H2O2![]() 本题解析: 本题解析:
本题难度:一般
5、填空题 ( 12分)
(1)二甲醚燃料电池的正极反应式为 。电池在放电过程中,负极周围溶液的pH 。(填“增大”、“减小” 或“不变”)
(2)以上述电池为电源,通过导线电解池相连。两极为石墨,电解质溶液为1L
0.1mol/LKCl溶液,写出电解总反应的离子方程式为 。
(3)室温时,按上述(2)电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸得到右图(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
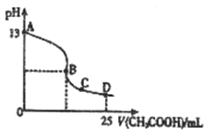
①若图中的B点pH=7,则滴定终点在 区间(填 “AB”、“BC”或“CD”)。
B点溶液中离子浓度大小为 。
②D点溶液中C(HAc) C(Ac_ )(填> 、< 或= )。
参考答案:(12分)(1)O2+4H++4e-=2H2O 减
本题解析:(1)原电池中负极失去电子,发生氧化反应,正极得到电子,发生还原反应。再氧气在正极通入,二甲醚在负极。所以正极的电极反应式是O2+4H++4e-=2H2O,负极电极反应式是CH3OCH3+3H2O=2CO2+12e-+12H+,因此电池在放电过程中,负极周围溶液的pH减小。
(2)惰性电极电解氯化钾溶液时,阳极是氯离子放电生成氯气,阴极是氢离子放电生成氢气,所以总的反应式是2Cl-+2H2O H2↑+Cl2↑+2OH-。 H2↑+Cl2↑+2OH-。
(3)①醋酸是弱酸,因此当醋酸与氢氧化钾恰好反应时,生成的醋酸钾水解,溶液显碱性。由于B点pH=7,所以滴定终点在AB之间;溶液显中性,根据电荷守恒定律可知,此时在B点离子浓度大小顺序是c(CH3COO-)=c(K+>c(H+)=c(OH-)。
②根据图像可知,氢氧化钾的浓度是0.1mol/L,所以D点溶液中含有的溶质是醋酸和醋酸钾。由于溶液显酸性,这说明醋酸的电离程度大于醋酸钾的水解程度,因此c(HAc)<c(Ac_)。
本题难度:困难
|