微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质反应后一定有+3价铁生成的是
①过量的Fe与Cl2反应;?????????
②Fe与过量稀H2SO4反应后,再向其中加入KNO3;?
③Fe(NO3) 2溶液中加入少量盐酸;
④Fe和Fe2O3的混合物溶于盐酸中。
A.只有①
B.只有①②
C.只有①②③
D.全部
2、填空题 (12分)向盛有5 mL 0.005 mol/L FeCl3溶液的试管中加入5 mL 0.01 mol/L KSCN?溶液,溶液呈红色。将上述溶液均分置于甲、乙两支试管中,向甲试管中加入4滴饱和FeCl3溶液,向乙试管中加入4滴浓KSCN溶液,充分振荡,观察溶液颜色变化。然后再分别向上述两支试管中滴加5滴0.5 mol/L NaOH溶液,观察现象并回答下列问题。
⑴向两支试管中分别加入饱和FeCl3溶液和浓KSCN溶液后,均可观察到的现象是__________________________________。
⑵产生上述现象后,向两支试管中滴加NaOH溶液,均可观察到的现象是_________
______________,产生该现象的原因是___________________________________。
⑶滴加NaOH溶液后,除观察到⑵中所述现象外,还会看到一支试管中有沉淀生成,另一支试管中几乎没有。有沉淀生成的试管是_________(填“甲”或“乙”)。
3、实验题 (10分)某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:(1)用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成 高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。
高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。

①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当________时(填实验现象),说明“铁与水蒸气”能够进行反应。
②写出铁与水蒸气反应的化学方程式_______________。
③实验中石棉绒的作用是????????????????????????????????。
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成气体的体积,计算出铁粉的转化率。
①收集并测量气体体积应选图中的________装置。
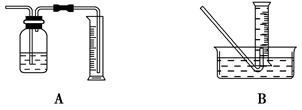
②称取0.24 g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088 g/L,最好选用______规格的量筒(选填字母序号)。
A.100 mL
B.200 mL
C.500 mL
D.1 000 mL
4、选择题 硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是
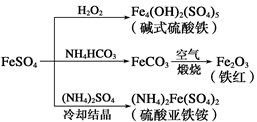
A.制备碱式硫酸铁利用了过氧化氢的氧化性
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质
5、填空题 (14分).以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4・7 H2O。
H2O。
Ⅱ.将FeSO4・7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
Ⅳ.将浊液过滤,用90 ℃热水洗涤沉淀,干燥后得到FeCO3固体。
Ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是_________________。
(2)Ⅱ中,需加一定量酸,该酸最好是????。运用化学平衡原理简述该酸的作用________________________________________________________________________。
(3)Ⅲ中,生成FeCO3的离子方程式是___________________________________________
若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是_______________________________________。
(4)Ⅳ中,通过检验SO来判断沉淀是否洗涤干净,检验SO的操作是__________
________________________________________________________________________。
(5)已知煅烧FeCO3的化学方程式是4FeCO3+O22Fe2O3+4CO2。现煅烧464.0  kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g・mol-1:FeCO3 116 Fe2O3 160 FeO 72)
kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g・mol-1:FeCO3 116 Fe2O3 160 FeO 72)