微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (9分)向Fe3O4和 Fe的固体混合物6.88g中加入50ml 2 mol・L―1H2SO4,恰好使固体完全溶解,并放出一定量气体。在所得溶液中加入KSCN溶液,溶液不变红色。
(1)??????????????写出Fe3O4和稀H2SO4反应的化学方程式______________________________。
(2)??????????????混合物中Fe3O4和 Fe的物质的量(写出计算过程)。
(3)??????????????求反应中产生的气体在标准状况下的体积。(写出计算过程)。
若用足量的CO在高温下与相同质量的上述固体混合物反应,求最终能得到铁的质量。(写出计算过程)。
2、简答题 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%.目前我国已经在技术上取得突破--用硫酸渣炼铁.
I.某学生探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验(已知25℃氢氧化镁Ksp=5.6×10-12;氢氧化铁Ksp=3.5×10-38;一水合氨电离常数K=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol?L-1).
方案一:
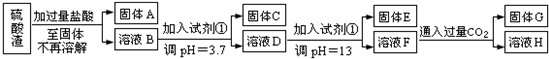
请回答:
(1)写出固体E的化学式:______.
(2)试剂①是______
A.氢氧化钠????B.氧化铝??????C.氨水????D.水
(3)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是______
A.石蕊试液????B.广泛pH试纸??C.精密pH试纸??D.pH计
(4)溶液H中溶质的化学式:______
(5)要将固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为______.
(6)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)=______.
方案二:
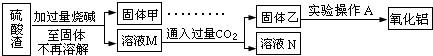
请回答:
(7)此方案的主要问题有:______
(8)写出由溶液M→固体乙这个过程中,最主要化学反应的离子方程式:______
II.为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(1)判断到达滴定终点的现象是______.
(2)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL,试样溶液,用1.000×10-2mol?L-1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00mL,则残留物中铁元素的质量分数是______.
3、填空题 将一定量的Fe粉、Cu粉、FeCl3溶液、CuCl2溶液混合于某容器中充分反应(假定容器不参与反应),试判断下列情况下容器中金属离子与金属单质的存在情况:
(1)若Fe粉有剩余,则容器中不可能有____________
(2)若FeCl3有剩余,则容器中不可能有___________
(3)若CuCl2有剩余,则容器中还可能有________________________
(4)若FeCl3和CuCl2都有剩余,则容器中还可能有______________
4、选择题 建筑用的红砖和青砖,其颜色是由其中含有的不同价态的铁氧化物所致。我国古代砖瓦建筑能够保持到现在的,几乎无一例外的是由青砖建成。有人提出以下可能的原因:
①青砖中含的是FeO;②青砖中含的是Fe3O4;③Fe2O3遇长期酸雨侵蚀会风化溶解使砖瓦强度降低;④Fe3O4性质稳定;⑤FeO性质稳定。你认为有道理的是
A.①③⑤
B.②③④
C.③⑤
D.①②③④⑤
5、填空题 (8分)根据下列流程处理废旧电路板,回收金属M,并制得高效绿色净水剂K2EO4。
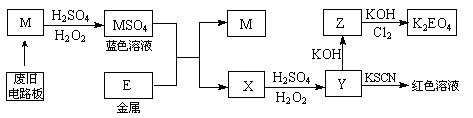
据此回答问题:
(1)M的化学式是????。
 (2)M?????MSO4过程中,氧化剂是????,还原剂是????。
(2)M?????MSO4过程中,氧化剂是????,还原剂是????。
(3)写出Z→K2EO4的化学反应方程式:?????????。
(4)向Y溶液中滴加KI淀粉溶液,变为蓝色,其原因用离子方程式解释为:????。
(5)控制其他条件相同,印刷电路板的金属 M用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下金属M的平均溶解速率(见下表)。
温度(℃)
| 20
| 30
| 40
| 50
| 60
| 70
| 80
|
V(M)(x10-3mol.L-1.min-1)
| 7.34
| 8.01
| 9.25
| 7.98
| 7.24
| 6.73
| 5.76
当温度高于40℃时,M的平均溶解速率随着反应温度升高而下降,其主要原因是??。
|