微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:
C 2―+2e―→C,B―2e―→B2+则A、B、C、D金属性由强到弱的顺序为(??)
A.A>B>C>D????? B.A>B>D>C????C.D>A>B>C???????? D.D>C>A>B
2、填空题 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如下图所示装置.试回答下列问题:
(1)若电解质溶液为稀硫酸,则Zn棒为原电池的______极,可观察到Cu棒的所产生现象是______,试用电极反应式表示该现象:______.
(2)若电解质为硫酸铜溶液,则Cu棒上发生______反应,Zn棒上发生反应的电极反应式为:______.
(3)若在上述两个过程中,Zn棒减少的质量相等,则Cu棒上(1)和(2)所析出物质的质量之比为:______.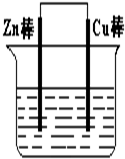
3、选择题 下列说法中正确的是
A.同一可逆反应使用不同的催化剂时,高效催化剂可增大平衡转化率
B.已知反应SO2(g)+H2O(g)=H2SO3(l),该过程熵值增大
C.下图可表示爆炸反应的能量变化曲线
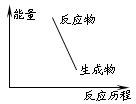
D.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H不同
4、简答题 某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题:

(1)如图是干电池的基本构造图,干电池工作时正极上的反应是N
H
+4
+e-=NH3↑+1
2
H2↑则负极上的电极反应式是______.MnO2的作用是除去正极上的某产物,本身生成Mn2O3,该反应的化学方程式是______.
(2)锌皮和碳棒的回收:用钳子和剪子剪开回收的干电池的锌筒,将锌皮和碳棒取出,刷洗干净,将电池内的黑色粉末移入小烧杯中.
(3)氯化铵、氯化锌的提取、分离和检验.①如何从黑色粉末中提取NH4Cl和ZnCl2的晶体混合物?写出简要的实验步骤:______.
②用什么方法可将NH4Cl和ZnCl2的晶体混合物分离开?______.
③写出证明ZnCl2晶体中含Zn2+的操作步骤及实验现象:______(已知Zn(OH)2是两性氢氧化物且能溶解于氨水)
④最后剩余的黑色残渣的主要成分是MnO2,还有炭黑和有机物等,可用灼烧的方法除去杂质.该实验中需要用到的主要仪器除酒精灯外,还有______.
5、选择题 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是

A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:BH4-+ 8OH-+8e-→BO2-+ 6H2O
D.每消耗3 mol H2O2,转移的电子为3 mol
|