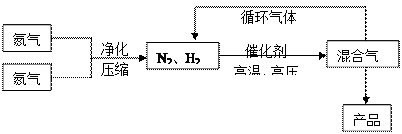微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是
A.将水加热煮沸,测得pH=6
B.向纯水中投入一小块金属钠
C.向水中加入NH4Cl固体
D.向水中加入Na2CO3固体
2、填空题 373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应: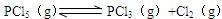 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。
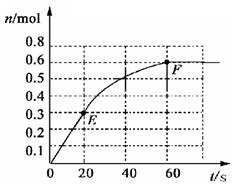
(1 )前 20
)前 20 s内 PCl5(g)的平均反应速率为??????
s内 PCl5(g)的平均反应速率为??????
(2)373K时该反应的平衡常数的值为???????
(3)若在此平衡体系中再加入 1mol的 PCl5,与原平衡比较,新平衡时 PCl5的转化率???(填“增大”或“减小”,下同)。PCl5的平衡浓度???????????????????。
(4)将原平衡升温至 473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”)????????,为增大平衡体系中 Cl2的物质的量,下列措施正确的是(其它条件相同)?????
a.升高温度???????????????????????????? b.扩大容器的体积
c.加入合适的催化剂???????????????????? d.再充入 PCl3
3、选择题 下列化学反应中,为使平衡体系析出更多的银,可采取的措施是Ag++Fe2+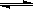 Ag(固)+Fe3+(正反应放热)
Ag(固)+Fe3+(正反应放热)
A常温下加压 B增加Fe3+的浓度
C增加Fe2+的浓度 D移去一些析出的银
4、填空题 (15分)氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g) 2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下:
2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下: