��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ��Σ����������д�����������һ�ִ��������Ĺ�ҵ���̣�
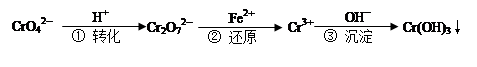
����˵����ȷ���ǣ�
A���ı䷴Ӧ�ٵ�ƽ����ϵ��c(H+)Ũ�ȣ���Һ��ɫ�����Ա仯
B����2v (Cr2O72��) ="v" (CrO42��)��˵����Ӧ�ٴ�ƽ��״̬
C����Ӧ���л�ԭ1mol Cr2O72������Ҫ6 mol��Fe2+
D��FeSO4��Һ�����Ե�ԭ����Fe2++ 2H2O  Fe(OH) 2��+ 2H+
Fe(OH) 2��+ 2H+
�ο��𰸣�C
���������
������������ݻ�ѧƽ��Ӱ�����ط�����������Ũ������ƽ��������У���Һ��ɫ�����仯�����ɫ��������Ũ�ȼ�Сƽ��������У���Һ�ʻ�ɫ����A����ѧ��Ӧ����֮�ȵ��ڻ�ѧ����ʽ�м�����֮�ȣ�������Ӧ����֮�ȣ�����֤����Ӧ�ﵽƽ�⣬��B��������������ԭ��Ӧ�����غ���㣬Cr2O72������2Cr3����6e����Fe2����Fe3����e������ԭ1mol Cr2O72������Ҫ6mol��Fe2������C��ȷ����������ˮ��̶�����������������������������Ӧ�����ǿ��淴Ӧ����Ӧ�����ӷ���ʽΪ��Fe2��+2H2O?Fe��
�����Ѷȣ�һ��
2��ѡ���� ȡ��ͬ�����KI��Na2S��FeBr2��Һ���ֱ�ͨ��������Cl2������Ӧǡ�����ʱ������Cl2�������ͬ��ͬ�¡�ͬѹ�����£�����KI��Na2S��FeBr2��Һ�����ʵ���Ũ��֮����
��??��
A��1��1��2
B��2��1��3
C��6��3��2
D��3��2��1
�ο��𰸣�C
���������
�����������Ϊ���ĵ������������ȣ�����ڷ�Ӧ�еõ��ĵ��ӵ����ʵ�������ȵģ���ô��Ϊ��ԭ�������������ʣ��ڷ�Ӧ����ʧȥ�ĵ�����Ҳ����ȵģ�1 mol KI��ת��ɵ���ʱ��ʧȥ1 mol�ĵ��ӣ���1 mol Na2S������ʱ��ʧȥ2 mol���ӣ�1 mol FeBr2������ʱ��ʧȥ3mol���ӣ���Ϊ�ڷ�Ӧ���������õ��ĵ�����ȣ��������ĵ�KI��Na2S��FeBr2�ֱܷ���6 mol��3mol��2 mol������Ϊ��ͬһ��Һ�У�����KI��Na2S��FeBr2��Һ�����ʵ���Ũ��֮����6��3��2��ѡC��
�����Ѷȣ�һ��
3��ѡ���� ClO2��һ�ֹ����͵����������������绷�����˵�Ҫ��ClO2����ȡ��Cl2��Ϊ��������ˮ������������ҵ��ClO2����NaClO3��Na2SO3��Һ��ϲ���H2SO4�ữ��Ӧ�Ƶã�����Na2SO3������ΪNa2SO4�������Ϸ�Ӧ�У�NaClO3��Na2SO3�����ʵ���֮��Ϊ��???��
A��1�U1
B��2�U1
C��1�U2
D��2�U3
�ο��𰸣�B
���������
���������NaClO3��Na2SO3��Һ��ϲ���H2SO4�ữ��Ӧ�����У���Ԫ�ػ��ϼ���+5�۽���+4�ۣ�������1�ۣ���Ԫ�ػ��ϼ۴�+4�����ߵ�+6�ۣ�������2�ۣ����ϼ��������ͻ��ϼ۽�������ȣ�����NaClO3��Na2SO3�����ʵ���֮��Ϊ2��1��
��ѡB��
����������Ŀ����ѧ��������ԭ��Ӧ�еĵ����غ㶨�ɣ����Ը�����ѧ֪ʶ��������á�
�����Ѷȣ�һ��
4������� ﮱ���Ϊ�����ܽ���������ҵ�����������-﮻Կ�(LiAlSi2O6��������þ����)��250��300�淴Ӧ������Li2SO4�Լ����������MgSO4�ȣ��乤ҵ�����������£�
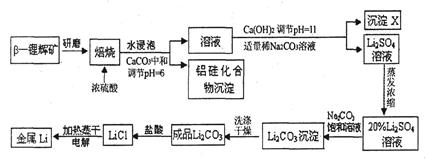
(1)����������ʽ��ʾLiAlSi2O6����ɣ�___________________��
(2)����X����Ҫ�ɷ���(д��ѧʽ)________________________��
(3)����������ʹ����N a2CO3��Һ����˵��ǰ��Ũ�Ȳ�ͬ��ԭ��:
a2CO3��Һ����˵��ǰ��Ũ�Ȳ�ͬ��ԭ��:
____________________________________________________________________��
(4)﮺������ڼ���ʱ�ܷ�Ӧ���ɰ�ɫ�����⻯ﮣ��⻯�����ˮ�������ܽⲢ�ͷų����������塣��д���⻯���ˮ��Ӧ�Ļ�ѧ����ʽ��_____________________________________��
(5)��������Li2C03��ȫ��Ӧ�����Һ���������ɵõ����壬�ٽ������ڵ������ﮡ����ʱ�����������л��������������ԭ����__________________________________________��
�ο��𰸣�
 �����������
�����������
�����Ѷȣ�һ��
5������� �����������Ļ������ڹ�����ռ����Ҫ��λ���ϳɰ���ҵ�У��ϳ�����ÿ����2 mol NH3���ų�92��4 kJ������
��1������ʼʱ�������ڷ���2 mol N2��6 mol H2����ƽ���ų�������ΪQ����Q 184��8kJ���>������<����=������һ�������£����ܱպ��ݵ������У��ܱ�ʾ��Ӧ�ﵽ��ѧƽ��״̬���� ��
a��3v��(N2)=v��(H2�� b��2v��(H2)= v��(NH3��
c����������ܶȱ��ֲ��� d��c(N2)��c(H2)��c(NH3)=1��3��2
��ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]����Ӧ�Ļ�ѧ����ʽΪ
2NH3 (g)+ CO2 (g�� CO(NH2)2 (l��+ H2O (l)��
CO(NH2)2 (l��+ H2O (l)��
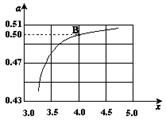
��2����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�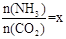 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
��3��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ ��
��4����֪�� 3Cl2+2NH3��N2+6HCl
�ο��𰸣�
���������
�����Ѷȣ�����