微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于盐酸与醋酸两种稀溶液的说法正确的是( )
A.相同物质的量浓度的两溶液中c(H+)相同
B.pH=3的两溶液稀释100倍,pH都为5
C.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠
D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
参考答案:C
本题解析:
本题难度:一般
2、填空题 写出下列物质在水中的电离方程式:
(1)Na2SO4????????????????(2)CH3COOH?????????????????????
参考答案: 本题解析:
本题解析:
试题分析:Na2SO4为强电解质,在水溶液中完全电离;醋酸是弱电解质,在水溶液中部分电离,故用可逆符号。
点评:强弱电解质是历年高考重点,考生可根据物质的分类来判断熟记哪些是强电解质、哪些是弱电解质。
本题难度:一般
3、选择题 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是
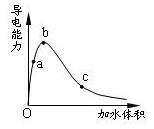
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b
C.a、b、c三点中b点n(H+)最大
D.a、b、c三点醋酸的电离程度:a<b<c
参考答案:D
本题解析:酸电离平衡为:CH3COOH CH3COO―+H+
CH3COO―+H+
冰醋酸加水稀释过程中,电离度一直在增大,但醋酸浓度一直在减小,而c(H+)=cα;从图中可看出c(H+)是先增大后减小。而c(H+)决定了溶液的酸碱性及导电能力。但在稀释过程中,CH3COOH的量不会改变,故中和时所耗氢氧化钠的量是不会改变的。
本题难度:一般
4、选择题 在相同温度时,100mL0.01mol?L-1的醋酸溶液与10mL 0.1mol?L-1的醋酸溶液相比较,下列数值中,前者大于后者的是( )
A.H+的物质的量
B.醋酸的电离常数
C.中和时所需NaOH的量
D.CH3COOH的物质的量
参考答案:A
本题解析:
试题分析:醋酸为弱电解质,浓度越大,电离程度越小,两种溶质的物质的量都为0.001mol,则100mL 0.01mol?L-1的醋酸溶液与10mL0.1mol?L-1的醋酸溶液相比较,H+的物质的量前者大,A正确;电离平衡常数只与温度有关,温度相同则电离平衡常数相同,故B错误;由于溶质n(CH3COOH)都为0.001mol,中和时所需NaOH的量应相同,故C错误;由于溶质n(CH3COOH)都为0.001mol,则和锌反应产生氢气的量相同,故D错误;答案选A
考点:弱电解质在水中的电离平衡
本题难度:一般
5、选择题 与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 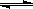 ??NH4++NH2-,据此判断以下叙述中错误的是:
??NH4++NH2-,据此判断以下叙述中错误的是:
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)・C(NH2-)是一个常数
C.液氨的电离到达平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)
参考答案:选C
本题解析:电离平衡状态是分子与离子浓度保持不变的状态,不是指分子与离子浓度相等,所以C 不正确。
本题难度:一般