微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在室温下,下列叙述正确的是( )
A.将1 mL 1.0×10-5 mol/L盐酸稀释到1000 mL,得到pH=8 的盐酸
B.将1 mL pH=3的一元酸溶液稀释到10 mL,若溶液的pH<4,则此酸为弱酸
C.用pH=1的盐酸分别中和1 mL pH="13" NaOH溶液和氨水,NaOH消耗盐酸的体积大
D.pH=2的盐酸与pH=1的硫酸比较,2 c(Cl― )=c(SO42― )
2、实验题 (9分)某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂。
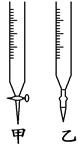
请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(2)用标准盐酸溶液滴定时,应将标准盐酸溶液注入________(填“甲”或“乙”)中。
(3)用标准的盐酸滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手轻轻摇动锥形瓶,眼睛注视_______________________________________________________。
(4)直到因加入一滴盐酸后,溶液颜色由________色变为________色,并在30 s内不变,即为终点。
(5)下列操作中可能使所测氢氧化钠溶液浓度偏大的是________。
A.酸式滴定管未用标准盐酸润洗,直接装入标准盐酸。
B.酸式滴定管滴定前有气泡,滴定后气泡消失。
C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥。
D.读取盐酸体积开始时仰视读数,滴定结束后俯视读数。
3、填空题 以下各题中各量的关系,请用“
4、选择题 在由水电离产生的c(H+)=1×10
5、选择题 25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba(OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是 [???? ]
A.1∶10∶1010∶109
B.1∶5∶5×109∶5×108
C.1∶20∶1010∶109
D.1∶10∶104∶109