微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 《科学》杂志评出2004年10大科技突破,其中“火星上‘找’到水的影子”名列第一.下列关于水的说法中正确的是( )
A.水的电离过程是吸热的过程
B.在水中加入酸,会促进水的电离
C.水是强电解质
D.升高温度,水的离子积常数会减小
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(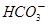 )的值保持增大
)的值保持增大
②浓度均为0.1mol・L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(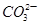 )+c(
)+c(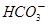 )]
)]
③在0.1mol・L-1氨水中滴加0.1mol・L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol・L-1
④向0.1mol・L-1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c( )、c(
)、c( )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+2c(H2S)+c(HS-)
A.①④
B.②④
C.①③
D.②⑤
参考答案:B
本题解析:
试题分析:①加水稀释,碳酸氢根的水解程度增大,所以比值增大,正确;②在同业中遵循物料守恒,钠原子:碳原子=3:2,所以有2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],错误;③恰好完全反应时,溶液中的氢离子和氢氧根离子都是水电离的,所以溶液的pH=a,则溶液中的氢离子浓度=10-amol/L,则氢氧根离子浓度也为10-amol/L,正确;④加入氢氧化钠固体,促进铵根离子水解,抑制亚硫酸根离子水解,所以铵根离子浓度减小,亚硫酸根离子浓度增大,错误;⑤根据溶液中质子守恒,即水电离的氢离子和氢氧根离子浓度永远相等,可以写出c(H+)=c(OH-)+2c(H2S)+c(HS-),正确;所以选B。
考点:溶液的酸碱性和溶液中的离子浓度比较
本题难度:困难
3、选择题 在25℃时,某稀溶液中由水电离产生的c(OH-)水=10-11mol/L。下列有关该溶液的叙述正确的是
A.该溶液一定呈酸性
B.该溶液中的c(H+)肯定等于10-3mol/L
C.该溶液的pH可能为3,可能为11
D.该溶液一定呈碱性
参考答案:C
本题解析:
试题分析:根据水的离子积常数,可知由水电离出的c(H+)=c(OH-)=10-13 mol・L-1,这是由于在水中加酸或加碱,抑制了水的电离。若水中加酸,溶液呈酸性,则溶液中OH-只来自水的电离,c(H+)水=c(OH-)水=c(OH-)液=10-13 mol・L-1,由KW=c(H+)液・c(OH-)液得:c(H+)液=10-14/10-13=10-1 mol・L-1,pH=1,若水中加碱,溶液呈碱性,则溶液中H+只来自水的电离c(H+)液=c(H+)水=10-13 mol・L-1,pH=13。
考点:考查水的电离平衡。
本题难度:一般
4、选择题 向水中分别加入下列溶液,对水的电离平衡不产生影响的是
A.KHSO4溶液
B.KHCO3溶液
C.KHS溶液
D.KI溶液
参考答案:D
本题解析:
试题分析:KHSO4溶液电离出大量氢离子,抑制水的电离,故A错误;KHCO3溶液中,HCO3-水解能促进水电离,故B错误;KHS溶液,HS―水解程度大于电离,能促进水电离,故C错误;KI溶液为强酸强碱盐,故D正确。
考点:本题考查水的电离。
本题难度:简单
5、选择题 将pH=6的CH3COOH溶液加水稀释1000倍后,溶液中的( )
A.pH=9
B.c(OH-)≈10-5 mol・L-1
C.pH≈7
D.c(OH-)<10-7 mol・L-1
参考答案:C
本题解析:将pH=6的CH3COOH溶液加水稀释1000倍后,溶液pH不等于9,此时溶液接近中性,pH≈7。
本题难度:一般