微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)操作I是配制溶液,所用到的玻璃仪器除烧杯、玻璃棒外,还必须有?????????????????????、?????????????????.(填仪器名称)
(2)下列操作可能使所配溶液浓度偏小的是________________(填写序号)。
①未洗涤烧杯和玻璃棒????????????????????????????
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水?
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子方程式??????????????????????????????????????????,
(4)检验沉淀是否已经洗涤干净的操作是???????????????????? ????????????????????。
(5)若原样品质量a为50g,加热后红棕色固体质量b为3g,则样品中铁元素的质量分数是??????????????????。
2、实验题 某课外活动小组设计了如下图所示的实验装置进行实验。回答下列问题:
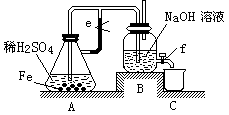
⑴ 开始实验时弹簧夹e是打开的,A中发生反应的离子方程式为:???????????????????,
B中可以观察到的现象是????????????????????????????????????????????。
⑵ 数分钟后夹上弹簧夹e,B中可以观察到的现象是??????????????????????????????。
⑶ 如果开启活塞f放掉2/3液体,B中可观察到的现象是??????????????????????????,
有关反应的化学方程式是??????????????????????????????????????????。
3、选择题 将FeO、Fe2O、Fe3O4混合物均分成两等份,在相同条件下,一份用足量H2还原,参加反应H2的体积为V1,另一份用足量浓NHO3处理得NO2(无其它还原性气体生成)气体体积为V2,若V1:V2=4:1(V1和V2均在相同条件下测定),测原混合物中各成分的物质的量之比可能为(???)
A.2:3:2
B.3:3:2
C.3:2:2
D.无法计算
4、选择题 农药波尔多液可用于水果灭虫,是由石灰水和硫酸铜溶液混合而成的悬浊液。它不能用铁制容器盛放,是因为铁与该农药中的硫酸铜起反应。在该反应中,对铁的叙述错误的是(???)
A.铁发生还原反应
B.铁发生氧化反应
C.铁是还原剂
D.铁失去电子
5、填空题 CuSO4・5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4・5H2O的实验室制备流程图。
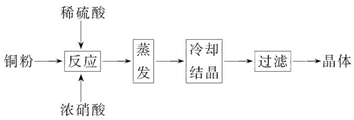
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:_____________、_____________。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4・5H2O中可能存在的杂质是_____________,除去这种杂质的实验操作称为_____________。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。称取0.100 0 g提纯后的CuSO4・5H2O试样于锥形瓶中,加入0.100 0 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用
0.100 0 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.100 0 g该试样中含CuSO4・5H2O_____________g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用_____________。