微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 草酸亚铁晶体(FeC2O4・2H2O)用作分析试剂及显影剂和新型电池材料磷酸亚铁锂的生产。回答下列问题:
I.兴趣小组对草酸亚铁晶体的分解产物进行实验和探究。探究分解得到的固体产物中铁元素的存在形式。
(1)提出假设
假设一:___________;???假设二:全部是FeO ;??????假设三:FeO和Fe混合物。
(2)设计实验方案证明假设三。
实验步骤
| 现象与结论
|
步骤1:向试管中加入少量固体产物,再加入足量?????????,充分震荡
| 若溶液颜色明显改编,且有???????生成,则证明有铁单质存在
|
步骤2:将步骤1中得到的浊液过滤,并用蒸馏水洗涤至洗涤液无色
| ?
|
步骤3:去步骤2得到少量固体与试管中,滴加
??????????????????
| ??????????????????????
?
限选试剂:稀盐酸、新制的氯水、0.1mol.L-1CuSO4溶液、20% KSCN溶液、蒸馏水。
Ⅱ.兴趣小组在文献中查阅到,FeC2O4・2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4・2H2O晶体受热分解的化学方程式为:_______________
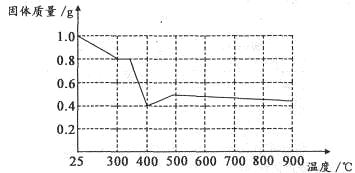
根据图象,如有1.0g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4g。某同学由此得出结论:假设二不成立。你是否同意该同学的结论,并简述理由:______________________。????????????
2、选择题
A.9.6 g
B.6.4 g
C.3.2 g
D.1.6 g
3、选择题 m g FeO、Fe2O3、CuO的混合物,加入120mL 1.0mol/L H2SO4溶液中完全溶解,向所得溶液中逐滴加入1.5mol/L NaOH溶液至刚出现沉淀时,消耗NaOH溶液40mL;将m g的混合物用CO气体加热还原,实验过程中耗去标准状况下的CO3.36升,得固体w g。则w的值为
A.m-0.96
B.m-1.44
C.m-1.6
D.m-2.4
4、填空题 判断存放的FeCl2溶液是否变质。从现象观察看????????????????????????????;鉴定的方法为加入?????????试剂,若溶液出现 ???????????????????????????????;则证明有????????????存在。实验室为了防止FeCl2溶液变质,在配制时常加入 ???? ??? 和 ????? 。向FeSO4溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象????????????????????????????????????????。 ???????????????????????????????;则证明有????????????存在。实验室为了防止FeCl2溶液变质,在配制时常加入 ???? ??? 和 ????? 。向FeSO4溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象????????????????????????????????????????。
5、选择题 当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成为深蓝色的溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀:将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色,根据上述实验现象分析推测,下列描述正确的有????????????????????????????????????(???)

A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子

B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应

C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下,只发生了氧化反应

D.反应过程中消耗的SO2与生成的SO2的物质的量相等
|