微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题
对可逆反应A2(g)+B2(g) 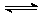 ?2AB(g) 在一定条件下,达到平衡状态的标志是( )
?2AB(g) 在一定条件下,达到平衡状态的标志是( )
A.平衡时容器内各物质的物质的量比为1∶1∶2
B.平衡时容器内的总压强不随时间而变化
C.单位时间内生成2n mol AB的同时,生成n mol的B2
D.单位时间内,生成n mol A2的同时,生成n mol的B2
参考答案:C
本题解析:平衡时容器内各物质的物质的量之比是没有规律的,只是各物质的物质的量浓度保持不变是一般规律,A错;对于反应前后气体不变的反应,容器内的总压强不随时间的变化而改变,无论是否平衡!B不能选择;对于C,D 类型需要了解六个字的“同边异,异边同”原理,对于D,如果反应向左进行,单位时间内,本来就是生成n mol A2的同时,一定生成了n mol的B2;对于C,表示反应向左进行的同时也在向右进行,而且程度相同!所以是正确的。
本题难度:一般
2、填空题 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:

(1)该反应所用的催化剂是_______(填写化合物名称),该反应450℃时的平衡常数______500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是________________。
(3)下列描述中能说明上述反应已达平衡的是____.
a.v(O2)正=2v(SO3)逆
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充人0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=___mo1・L-1・min-1 ;若继续通入0.20mol SO2和0.10 mol O2,则平衡____移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,___mol< n(SO3)<__mol。
参考答案:(1)五氧化二钒(V2O5);大于
(2)在450℃
本题解析:
本题难度:一般
3、选择题 已知反应2SO2(g)+O2(g)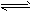 2SO3(g)ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入
2SO3(g)ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入
SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是
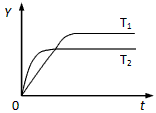
[???? ]
A.O2的体积分数
B.混合气体的密度
C.密闭容器内的压强
D.SO2的转化率
参考答案:D
本题解析:
本题难度:一般
4、选择题 在容积可变的密闭容器中,2 mol N2和8 mol H2在一定条件下反应,达到平衡时,H2的转化率为25%,则平衡时氨气的体积分数接近于
A.5%
B.10%
C.15%
D.20%
参考答案:C
本题解析:
试题分析:根据题意可列三段式的:
N2 + 3H2 2NH3
2NH3
起始状态 2mol 8mol 0
反应过程 1/3×8×25% 8×25% 8×25%×2/3
平衡状态 2-1/3×2 6 2×2/3
故平衡时氨气的体积分数为:(2×2/3)÷(2-1/3×2+6+2×2/3)≈15%,故C项正确。
考点:化学平衡计算。
本题难度:一般
5、简答题 一定温度下,在容积为V?L的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:
(1)该反应的反应物是______.
(2)该反应的化学反应方程式为:______;
(3)t1到t2时刻,以M的浓度变化表示的平均反应速率为:______
(4)若达到平衡状态的时间是2?min,N物质的平均反应速率为1.5mol?L-1?min-1,则此容器的容积为V=______L.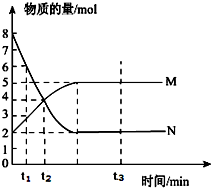
参考答案:(1)由图象可知,随着反应进行,N的物质的量减少,M的物质的
本题解析:
本题难度:一般