微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g) +H2O(g)=CO(g) +3H2(g) △H>0,在一定条件下,向体积为1L的密闭容器中充入1 mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是
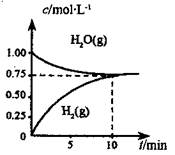
A.达平衡时,CH4( g)的转化率为75%
B.0~10 min 内,v(CO)=0.075 mol?L-1・min-1
C.该反应的化学平衡常数K=0.1875 mol?L-1
D.当CH4(g)的消耗速率与H2O(g)的生成速率相等,反应到达平衡
2、填空题 单质碘与红磷在常温下混合不反应,但滴入几滴水后能剧烈反应,生成HI和H3PO3。但实验室制取氢碘酸的方法是把H2S通入I2水中,过滤生成的硫,可得质量分数为50%的氢碘酸
(1)写出实验室制取氢碘酸的化学方程式______________________;
(2)氢碘酸在空气中放置易易氧化变质,写出可能发生反应的化学方程式___________________________;
(3)为防止氢碘酸在空气中氧化变质,可在氢碘酸中加入少量___________,写出有关反应的化学方程式__________________________。??????
(4)在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表:
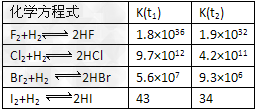
①已知t2>t1,HX的生成反应是__________?反应(填“吸热”或“放热”)。
②共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是_______________。
③仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_________________(选填字母)。
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱????
d.HX的稳定性逐渐减弱
3、填空题 氨气是一种重要的化工产品,是生产铵盐、尿素等的原料。工业合成氨的反应如下:N2(g) +3H2(g)  2NH3(g)??△H=一92. 4 KJ・mol-1
2NH3(g)??△H=一92. 4 KJ・mol-1
(1)2NH3(g)  N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有
N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有
①单位时间内生成3n mol H2:同时生成2n mol NH3②用NH3、N2、H2表示反应速率比为2∶1∶3 ③混合气体的密度不再改变 ④混合气体压强不再改变 ⑤混合气体平均相对分子质量不再改变
A.①③④
B.①②④⑤
C.①④⑤
D.②③④
(2)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2]。
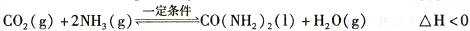
t℃时,向容积恒定为2L的密闭容器中加入0.10 molCO:和0. 40 molNH3 ,70 min开始达到平衡。反应中CO2 ( g)的物质的量随时间变化如下表所示: