微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)工业制硫酸时,利用接触氧化反应将SO2转化为SO3是一个关键的步骤。
(1)在接触室中2SO2(g)+O2(g)  2SO3(g)达到平衡状态的标志是______。
2SO3(g)达到平衡状态的标志是______。
A.υ(O2)正=2υ(SO2)逆
B.容器中气体的总质量不随时间而变化
C.容器中气体的颜色不随时间而变化
D.容器中气体的压强不随时间而变化
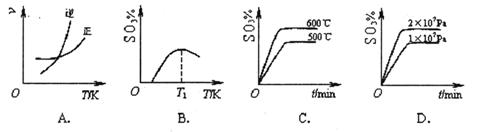
(2)下列关于反应2SO2(g)+O2(g)  2SO3(g) ΔH<0。下列图像中不正确的是______ (填字母序号)。
2SO3(g) ΔH<0。下列图像中不正确的是______ (填字母序号)。
(3)某温度下SO2(g)+  O2(g)
O2(g)  SO3(g) ΔH=-98KJ/mol
SO3(g) ΔH=-98KJ/mol
①开始时在体积固定的密闭容器中加入4mol SO2 (g)和1mol O2 (g),达到平衡时 共放出196 KJ的热量,该温度下SO2的平衡转化率为______
②已知固态单质硫的燃烧热为296KJ/mol,则由S(s)生成2 molSO3(g)的ΔH为____________
(4)检验SO42-常用BaCl2溶液。常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与2.0×10-3mol/L的H2SO4溶液混合。若要生成BaSO4沉淀,原BaCl2溶液的最小浓度为____________
2、选择题 在一定温度下,体积不变的密闭容器中可逆反应A(g)+3B(g)  2C(g) 达到平衡的标志是
2C(g) 达到平衡的标志是
A.气体的密度不再变化
B.A、B、C的浓度之比为1:3:2
C.A、B、C的浓度不再变化
D.单位时间内生成n molA,同时生成3n molB
3、填空题 将1molI2(g)和2molH2置于某2L密闭容器中,在一定温度下发生反应:
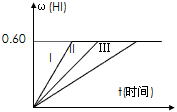
I2(g)+H2(g) 2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:(提示:同条件体积分数=物质的量分数)
2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:(提示:同条件体积分数=物质的量分数)
(1)达平衡时,I2(g)的物质的量浓度为________________。
(2)若改变反应条件下,在甲条件下ω(HI)的变化如图曲线(I)所示,在乙条件下ω(HI)的变化如图曲线(III)所示。则甲条件可能是________________(填入下列条件的序号。下同),乙条件可能是
________________。
① 恒容条件下,升高温度;② 恒容条件下,降低温度;③ 恒温条件下,缩小反应容器体积;
④ 恒温条件下,扩大反应容器体积;⑤ 恒温恒容条件下,加入适当催化剂。
(3)若保持温度不变,在另一相同的2L密闭容器中加入amol I2(g)、bmol H2和cmol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是:________________。
4、选择题 今有X(g)+Y(g)  2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是
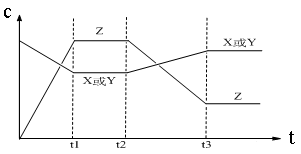
A.增大X或Y的浓度
B.增大压强
C.增大Z的浓度
D.升高温度
5、填空题 (10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1)?反应5min内,v(O2)=_________mol.L-1.min-1.
(2)?化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3)?判断该反应达到平衡的标志是_______________;
A.v消耗(SO2)=v生成(SO3)
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改 变
D.容器中气体的总物质的量不再变化