微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向某溶液中加入铝粉有H2产生,则在该溶液中一定能大量存在的离子组是
A.K+、Na+、Cl-、NO3-
B.OH-、CO32-、Cl-、K+
C.Fe2+、Na+、SO42-、NO3-
D.Cu2+、NO3-、NH4+、Cl-
参考答案:A
本题解析:加入铝粉有H2产生,该溶液中有大量的H+或OH-.B选项中的OH-、CO32-不能与H+大量共存.C选项中的Fe2+遇到OH-会生成沉淀,在酸性环境中会被NO3-氧化.D选项中的Cu2+、NH4+不能与OH-大量共存.
本题难度:简单
2、选择题 今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH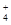 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO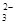 、SO
、SO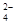 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH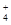 可能存在
可能存在
B.CO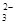 一定不存在
一定不存在
C.Na+一定存在
D.一定不存在Cl-
参考答案:C
本题解析:根据实验①可知,溶液中一定含有NH4+。氨气是1.36g,物质的量是0.08mol,则NH4+也是0.08mol;根据实验②可知,硫酸钡的质量是4.66g,碳酸钡的质量是12.54g-4.66g=7.88g,物质的量分别是0.02mol和0.04mol,则溶液中SO42-和CO32-的物质的量分别是0.02mol和0.04mol。所以溶液中一定没有Ba2+。根据溶液的电中性可知,溶液中一定还含有钠离子,但氯离子是不能确定的,选项C正确,答案选C。
本题难度:一般
3、选择题 下列离子方程式表示正确的是
A.AgNO3溶液中加入Cu:Cu + Ag+ = Cu2+ + Ag
B.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42―+Ba2++OH―==BaSO4↓+H2O
C.甲酸溶液滴到大理石台板上有气泡产生:2H+ + CaCO3 = CO2↑+ Ca2+ + H2O
D.等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合
参考答案:D
本题解析:试题分析:A、电荷不守恒,故错;B、H+、OH―、H2O的化学计量数应为2,故错;C、甲酸是弱酸,不能拆开,故错。故选D。
考点:离子方程式的正误判断
点评:离子方程式正误判断要注意:看原则:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。
本题难度:一般
4、填空题 某溶液甲中可能含有下列离子中的几种:K+、NO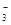 、SO
、SO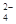 、NH
、NH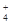 、CO
、CO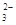 (不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为672mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
(1)甲溶液中一定存在的离子是??????????????????;
(2)甲溶液中一定不存在的离子是?????????????????;
(3)甲溶液中可能存在的离子是??????????????????????;你得出此结论的理由是????????????????????????????????????????????????。
参考答案:(1)NO 本题解析:
本题解析:
试题分析:(1)根据实验1:第一份加入足量的烧碱并加热,因NH4++OH-=NH3↑+H2O,会产生标准状况下为224mL气体,证明含有NH4+,且物质的量为0.01mol;
实验2:第二份先加入足量的盐酸,无现象,则一定不含有CO32-,再加足量的BaCl2溶液,得固体2.33g,证明一定含有SO42-,且物质的量为:n="m/M" ="2.33g/233g/mol" =0.01mol;根据溶液中的电荷守恒,溶液呈电中性,则一定含有钾离子,且钾离子的浓度≥0.01mol×2?0.01mol
本题难度:一般
5、选择题 同时对农作物施用含N、P、K的三种化肥,对给定的下列化肥①K2CO3、②KCl、③Ca(H2PO4)2、
④(NH4)2SO4,⑤氨水,最适当的组合是[???? ]
A.①③④
B.①③⑤
C.②③④
D.②③⑤
参考答案:C
本题解析:
本题难度:一般