微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子(不考虑难溶物自身的溶解),同时生成一种阴、阳离子个数比为1:1的白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是________.
A.Na+???????? B.Mg2+??????????C.Cu2+????????? D.Ag+
(2)三种正盐的化学式分别是:A???????????,B?????????,C???????????
(3) A、B、C同时溶于水时反应的离子方程式为??????????????????????????????
参考答案:(1) D(1分)
(2) FeCl3,AgNO3,K
本题解析:
试题分析:生成一种阴、阳离子个数比为1:1的白色沉淀,从给出的5种离子少了一种阳离子说明完全沉淀,白色沉淀不可能是硫酸盐(因为等物质的量正盐,如果是硫酸盐那么硫酸根离子就没有剩余)只能是氯化银,又根据阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序)B只能是硝酸银,氯离子有剩余所以A应是氯化铁,C既是硫酸钾。
本题难度:一般
2、选择题 下列各组离子能够大量共存的是
A.pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42-
B.水电离出的c(H+)=1×10-13mol・L-1的溶液中:K+、HCO3-、Cl-、S2-
C.使pH试纸显蓝色的溶液中:Cu2+、Fe3+、NO3-、SO42-
D.在AlCl3溶液中:Na+、[Al(OH)4]-、SO42-、NO3-
参考答案:A
本题解析:试题分析:A项, pH=0的溶液呈强酸性,上述离子可共存;B项,c(OH-)=1×10-1mol・L-1溶液强碱性,HCO3-不能存在;C项,溶液碱性,Cu2+、Fe3+不能存在;D.在AlCl3溶液显酸性,[Al(OH)4]-不能存在。
考点:离子共存
点评:判断离子是否可以共存,应从溶液的酸碱性,以及离子间是否发生反应着手。
本题难度:简单
3、选择题 下列用来表示物质变化的反应式中,错误的是
A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e-= 4OH-
B.向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+ 2 H+ + Ba2+ + 2OH-= BaSO4↓+ 2 H2O
C.明矾水解的离子方程式:Al3+ + 3H2O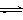 Al(OH)3 + 3H+
Al(OH)3 + 3H+
D.K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3 + 6HClΔK37Cl + 3Cl2↑+ 3H2O
参考答案:D
本题解析:
试题分析:A.钢铁腐蚀时可能发生吸氧腐蚀,其正极反应:2H2O+O2+4e-=4OH-,故A正确;B.向KHSO4溶液中滴入Ba(OH)2溶液使pH=7的离子反应为SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O,故B正确;C.明矾水解的离子方程式为Al3++3H2O?Al(OH)3+3H+,故C正确;D.K37ClO3与浓盐酸(HCl)在加热时生成氯气的反应为2K37ClO3+12HCl 本题难度:一般
本题难度:一般
4、选择题 下列各组中,离子能大量共存的是
A.NH4+、 Na+ 、SO42-、OH-
B.NH4+、H+、 Cl-、CO32-
C.K+、 NH4+、 NO3-、 Cl-
D.Ca2+、NH4+、NO3-、CO32-
参考答案:C
本题解析:离子间如果发生化学反应,则不能大量共存,反之可以。A中NH4+和OH-不能大量共存,B中H+和CO32-不能大量共存,D中Ca2+和CO32-不能大量共存,所以正确的答案选C。
本题难度:一般
5、选择题 下列反应中,既属于氧化还原反应,又属于离子反应的是(??? )
A.铝片与稀盐酸的反应
B.甲烷与氧气的反应
C.灼热的炭与二氧化碳反应生成一氧化碳
D.氢氧化钠溶液与稀盐酸的反应
参考答案:A
本题解析:
试题分析:A、正确;B、甲烷与氧气的反应,是分子反应,错误;C、灼热的炭与二氧化碳反应生成一氧化碳,是分子反应,错误; D、不是氧化还原反应,是离子反应,错误。
本题难度:一般