微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)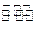 Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为?????????。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变???????????????????????????????????? b.容器内气体密度保持不变
c.c(H2)=c(H2O)??? d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡:????????②加入少量灼热的碳粉,则平衡:__???
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性___??_,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是????????。
2、填空题 将1molCO和1molH2O充入某固定容积的反应器中,在某条件下达到平衡:
CO+H2O(g)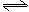 CO2+H2,此时有2/3的CO转化为CO2。
CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为???????????
(2)若容器体积为1L,到达平衡所需时间为2分钟,则H2的平均反应速率为?????????
(3)若在相同条件下,向容器中充入1molCO2、1molH2和1molH2O,则达到平衡时与⑴中平衡相比较,平衡应向????????(填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的??????
A.22.2%
B.27.55%
C.33.3%
D.36.8%
(4)结合(3)中计算结果分析若平衡向正方向移动时,则下列说法中正确的是(???)
①生成物的产量一定增加;??????????????②生成物的体积分数一定增加;
③反应物的转化率一定增大; ????????????④反应物的浓度一定降低;
⑤正反应速率一定大于逆反应速率;???????⑥一定使用了催化剂.
3、填空题 在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如下图,据图回答下列问题:
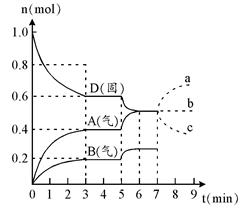
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为??????????。
(2)根据右图写出该反应的化学方程式??????????。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如右图,则该反应是??????(填“放热”或“吸热”)反应。若在第7分钟时增加D的物质的量,A的物质的量变化正确的是_____(用图中a~c的编号回答)
(4)某同学在学习了“化学反应速率和化学平衡”专题后,发表如下观点,你认为错误的是??????????。
a.化学反应速率理论是研究怎样在一定时间内快出产品
b.化学反应速率理论是研究怎样提高原料转化率
c.化学平衡理论是研究怎样使用有限原料多出产品
d.正确利用化学反应速率和化学平衡理论都可以提高化工生产的综合效益
4、填空题 1200℃时可用反应 2BBr3(g)+ 3H2(g)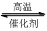 2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空:
2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空:
(1)下列说法能说明该反应达到平衡的是______(选填序号,下同)。
a. v正(BBr3)= 3v逆(HBr)????????????? b. 2c(H2) = c(HBr)
c.密闭容器内压强不再变化?????????? d. 容器内气体平均摩尔质量不再变化
(2)若密闭容器体积不变,升高温度,晶体硼的质量增加,下列说法正确的是_________。
a. 在平衡移动时正反应速率先增大后减小
b. 在平衡移动时逆反应速率始终增大
c. 正反应为放热反应
d. 达到新平衡后反应物不再转化为生成物
(3)若上述反应在10L的密闭容器内反应,5min后,气体总质量减少1.1 g,则该时间段内氢气的平均反应速率为__________________。
(4)往容器中充入0.2 mol BBr3和一定量H2,充分反应达到平衡后,混合气体中HBr百分含量与起始通入H2的物质的量有如图关系。在a、b、c三点中,H2 的转化率最高的是______(选填字母)。b点达到平衡后,再充入H2使平衡到达c点,此过程中平衡移动的方向为__________(填“正向”、“逆向”或“不移动”)。
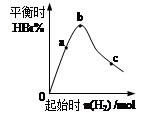
5、实验题 (18分)铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
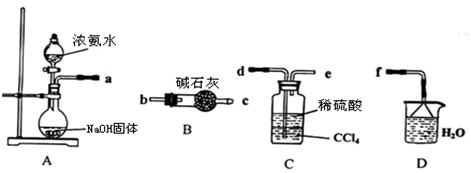
(1)仪器连接的顺序(用接口序号字母表示)是:a????????????????
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:?????????????????????????
??????????????????????????????????????????????????????。
(3)将装置C中两种液体分离开的操作名称是???????????????。
(4)(NH4)2SO4“低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意????????????????。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
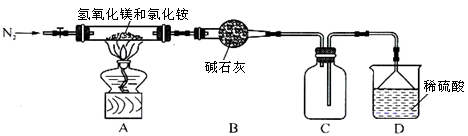 ?
?
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为??????????????????????????。
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,
二是?????????????????????????????????????????????。
(3)由MgCl2溶液蒸发得到MgCl2・6H2O晶体,蒸发的目的是_________。
a.得到热饱和溶液??????b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:???????????????????????????
????????????????????????????????????????????。
②由MgCl2・6H2O制备无水MgCl2的操作在?????????????氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。