微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Fe、Cu都是人类最早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
⑴ 甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到盛Cl2的集气瓶中。你认为甲同学在实验中应该观察到的现象是?;
⑵ 乙同学为验证Fe能和热的浓HNO3反应,设计了如下图所示的实验装置,请你指出装置中的不足之处?;?;
?。

⑶ 丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解。
丙同学依据反应现象得出Cu片溶解的原因可能是和HNO3发生反应。他依据的反应现象是?;请写出Cu片和稀HNO3反应的离子方程式?
你认为Cu片溶解的不同于丙同学的理由是?
⑷ 请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象?
?。
参考答案:(1)Cu在Cl2中燃烧,产生棕色烟(1分)
(2)试管中的液体超过试管容积的三分之一(1分);加热液体的试管应与桌面成45°角向上倾斜而不应垂直向上(1分);尾气吸收装置容易发生倒吸(1分)
(3)①试管上部出现红棕色气体或无色气体(1分)?②3Cu+2NO3-+8 H+=3Cu 2++2NO+4 H2O (2分),反应产生的Fe3+也能和Cu反应而使Cu片溶解(2分)
(4)取该溶液少许,滴加适量的KSCN溶液,不出现血红色,再滴加适量新制氯水,出现血红色(2分)
本题解析:略
本题难度:简单
2、实验题 某研究性学习小组设计实验方案制备氯化铜并验证次氯酸的漂白性。
已知氯化铜遇水蒸气潮解。
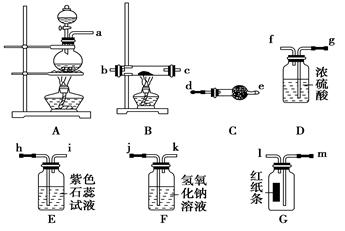 根据上述仪器组合装置,回答下列问题:
根据上述仪器组合装置,回答下列问题:
(1)组装实验装置:气体流向从左至右,导管口的连接顺序为__________________。
(2)为了防止空气与铜粉反应,先点燃________处酒精灯,当___________________时,再点燃另一酒精灯。
(3)D装置的作用是________________________,
F装置的作用是_________________ __________。
__________。
(4)能证明氯气没有漂白性,次氯酸有漂白性的实验现象________________________________________________________________________。
(5)本实验方案没有除去氯气中的氯化氢,对实验有无影响?________;理由是
_______________________________________________________________________ _。
_。
参考答案:(1)a→gf→bc(cb)→ml→hi→jk (3分)
(2)A B管充满黄绿色气体?(2分)
(3)干燥氯气; 吸收氯气,防止氯气污染环境(4分)
(4)G装置中红纸条没有明显变化;E中紫色石蕊试液先变红后褪色(4分)
(5)无影响 铜不与氯化氢反应(2分)
本题解析:略
本题难度:一般
3、实验题 (10分)某化学课外小组用右图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。
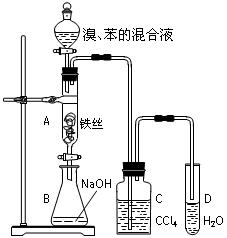
(1)写出A中反应的化学方程式:________________________________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_________________________。
(3)C中盛放CCl4的作用是_____________________________。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,通常有两种方法,请按要求填写下表。
?
| 向试管D中加入的试剂
| 能证明苯与液溴发生取代反应的现象
|
方法一
| ?
| ?
|
方法二
| ?
| ?
参考答案:(10分)(1)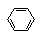 +Br2 +Br2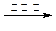 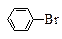 +HBr +HBr
(2)除去溶于溴苯中的溴?
(3)除去溴化氢气体中的溴蒸气
(4)方法一:AgNO3溶液?产生(淡黄色)沉淀
方法二:石蕊试液?溶液变红色(或其他合理答案)
(除第⑷小题每空1分,其余每空2分,共10分)
本题解析:略
本题难度:简单
4、选择题 下列装置或操作正确的是( )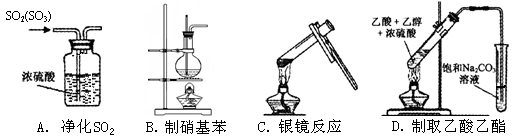
参考答案:A
本题解析:
答案:A
A、正确;B、水浴加热;C、水浴加热;D、导管不能插入饱和Na2CO3溶液中。
本题难度:一般
5、选择题 某学生用质量为a g、边长为b cm的正方形镀锌铁片与过量盐酸反应测定镀层厚度,并将实验结果绘图示意,反应完毕后铁片质量为c g(已知锌的密度为ρ g/cm3)。下列叙述错误的是
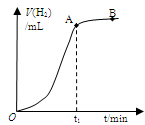
A.t1时刻锌镀层已完全反应
B.锌镀层的厚度为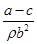
C.反应放热也是影响OA段的反应速率的因素之一
D.有原电池反应发生,正极的电极反应式为Zn - 2e → Zn2+
参考答案:BD
本题解析:A、锌活泼性强,且形成原电池反应速率快,其反应结束时铁与稀盐酸反应速率慢,正确;B、该实验原理是根据产生氢气的速率变化确定锌反应完成,根据铁片前后质量变化得出金属锌的质量,再有铁皮面积计算锌镀层的厚度,要注意铁片两面镀锌,故结果是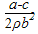 ,错误;C、金属与酸反应放热,反应速率加快,正确;D、有原电池反应发生,负极的电极反应式为Zn - 2e → Zn2+,错误。 ,错误;C、金属与酸反应放热,反应速率加快,正确;D、有原电池反应发生,负极的电极反应式为Zn - 2e → Zn2+,错误。
本题难度:一般
|