��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� 20.6gNH4HCO3��NaHSO3�ĸ����״�����ü��ȷֽ��ʵ�鷽�����ⶨNH4HCO3��������������֪��NaHSO3����ʱ�����SO2��������ͼ��ʾ����������ʢ�Լ���գ�
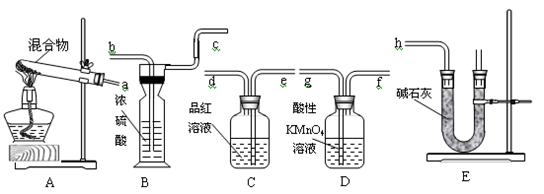
��1����������������ҵķ�������������˳��(��a��h��ʾ)Ϊ____________________��
��2������B������Ϊ_________��Eװ���зż�ʯ�ҵ���������Ϊ________��A��Eװ���ж��õ�����������Ϊ__________��
��3��D��������_______________________________________________________��
��4��C��������_________________________________����Cƿ����Һ��ɫ�б仯����ⶨ������ܻ�ƫ__________��
��5��B��������_____________________________________��
�ο��𰸣���1��agfedbch?��2��ϴ��ƿ��U�ιܣ�����̨
��3����ȥSO2���Է�ֹSO2�Բⶨ������Ӱ��
��4������SO2�Ƿ�������ȫ?��?��5������ˮ����?��ÿ��2�֣���16�֣�
�����������
�����Ѷȣ���
2������� ��15�֣�ij�������д�����CuS���������������P��������������������ʡ�ij��ѧ����С������������̣�ȡ�ÿ���Ϊԭ������CuC12��2H2O ���塣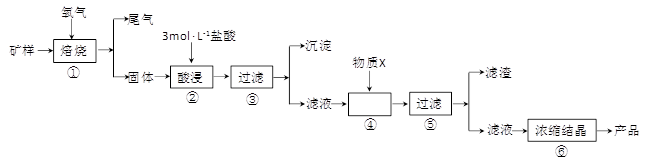
��֪�������£��������ӿ�ʼ�����ͳ�����ȫʱ��pH ���±���
��������
| �������↑ʼ������pH
| �������������ȫ��pH
|
Fe2+
| 7.0
| 9.0
|
Fe3+
| 1.9
| 3.2
|
Cu2+
| 4.7
| 6.7
|
�ش��������⣺
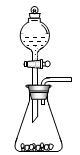
��l������ٵı��չ�������Ҫͨ����������ʵ�����У���ʹ�ó�����ѧ����������ͼ��ʾװ����ȡ��������д����Ϥ�ķ�������������������ѧ����ʽ��______________________��______________________��
��2�����ղ�����β���к��е�һ���������γ��������Ⱦ�����β��ͨ�백ˮ�У��ܷ��������Ӧ��д�����п��ܷ���������������ԭ��Ӧ�Ļ�ѧ����ʽ��____________________��__________________��
��3���������������У���Ҫ�õ�3 mol �� L-1������100 mL�����Ƹ�������Һʱ�������õ��ձ�������������ͷ�ι��⣬����Ҫ��������_______________________________________��
��4������ܼ�������X��Ŀ����_________________________________________������X ����ѡ�����������е�______________________��
��A����������?��B��ϡ����?��C����ˮ?��D������ͭ
��5������Һ�н�������Ũ�ȵ���1��10-5 mol �� L-1ʱ����Ϊ�ý������ӳ�����ȫ����Ksp[Fe(OH)2]=_____��
�ο��𰸣���1��2H2O2 ="==" 2H2O + O2 ����2Na2O2 + 2H2O ="==" 4NaOH + O2 ����
��2��2H2SO3+O2=2H2SO4��2(NH4)2SO3+O2=2(NH4)2SO4��2NH4HSO3+O2=2NH4HSO4?
��3��100 mL����ƿ����Ͳ��
��4��������Һ��pH��ʹFe3+��Fe(OH)3��������ʽ������D��
��5��1��10-15��
�����������1������װ��ͼ��֪�ǹ�Һ�����������壬������H2O2��Na2O2����ȡO2��Ӧ����ʽΪ��2H2O2 ="==" 2H2O + O2 ����2Na2O2 + 2H2O ="==" 4NaOH + O2 ������2��β���к��е���SO2��SO2û��ǿ�����Բ�����NH3����������ԭ��Ӧ��SO2�н�ǿ�Ļ�ԭ�ԣ����Ա������е�O2�����������Կ��ܷ�����������ԭ��ӦΪ2H2SO3+O2=2H2SO4��2(NH4)2SO3+O2=2(NH4)2SO4��2NH4HSO3+O2=2NH4HSO4��3������3mol �� L-1������100 mL�����õ��ձ�������������ͷ�ι��⣬����Ҫ��������100 mL����ƿ����Ͳ����4�������������↑ʼ��������ȫ������pH��֪��ֻҪ����pHֵ���Ϳ���Fe3+��Fe(OH)3��������ʽ�������ﵽ���ӵ�Ŀ�ġ�Ϊ�˲����������ʣ����ܵ���pHֵ������ѡͭ���������CuO��Cu(OH)2��CuCO3�ȡ���5��Fe(OH)2��ȫ������pH��9.0������Ksp[Fe(OH)2]=c(Fe2+)��c2(OH-)=1��10-5��(1��10-5)2=1��10-15��
��������������ʵ�������۵Ľ�ϣ��Ѷ����У��߿��е������⡣
�����Ѷȣ�һ��
3��ʵ���� �������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ���
�����Թ��м���3 mL 1 mol/L NaOH��Һ��3 mL �����飬�����ȡ�
��1�����ʵ��֤������ʵ�������������Br�����Br��? ����˵������ʵ�������Ԥ�������ʵ������
��2���۲쵽? ����ʱ��������������NaOH��Һ����ȫ��Ӧ��
��3���������������Ҵ��Ľṹ�����õIJ�����? ��? ��
�����Թ��м���3 mL NaOH�Ҵ���Һ��3 mL �����飬�����ȡ�
��4�����ʵ��֤������ʵ���������鷢��������ȥ��Ӧ? ����˵������ʵ�������Ԥ�������ʵ������
�ο��𰸣���1��ȡ������Ӧ����Һ�������Թ��У������м��������ϡ���ᣬ������Һ�еμӼ���AgNO3����������ɫ����?
��2���Թ�����Һ���úֲ�?
��3��������ף��˴Ź�������?
��4����������Ӧ���ɵ�������ͨ��ʢ��ˮ���Թܣ���ͨ��ʢ��KMnO4��Һ���Թܣ�KMnO4��Һ��ɫ����ֱ��ͨ����ˮ��������Ȼ�̼��Һ��
���������
�����Ѷȣ�һ��
4������� ����ϡ���������������Һ�����кͷ�Ӧ��ʵ��ʱ����Ӧ��������Һ�����ȱ仯��ͼ��ʾ��

��1���÷�Ӧ�Ļ�ѧ����ʽ____________________________.
��2����ʵ������ǽ�_______________�μӵ�___________��һ����Һ�С�
��3����������Һ������Ϊagʱ��������Һ�е�����Ϊ______________��д��ѧʽ����
��4����������Һ������Ϊbgʱ����������Һ�еμӷ�̪��Һ����Һ��_____________ɫ��
�ο��𰸣���1��NaOH+HCl=NaCl+H2O
(2) NaOH ��HCl?��3��NaCl��HCl?��4����
���������������ѧ����Ϥ���кͷ�Ӧʵ��Ϊ�زģ������˴Ĵ��£�һ��������ͼ��ʾ��Ӧ��������Һ��pH�仯��������ǽ��кͷ�Ӧʵ������Һ֪ʶ���ϡ������֪ʶ�л�ѧ����ʽ����д����Ӧ��������Һ��ɵ��ж��Լ���̪�ڼ�����Һ�г��ֵ���ɫ�ȡ�Ҫ��ѧ���н�ǿ��ʶͼ������˼ά����������������������ʵ���ѧ�����𡣱��������ѶȽϴ�4�����нϺõ��ݶȣ������ѧ���Ļ����Ժͷ�չ�ԣ����нϺõ�ѡ�ι��ܡ�
��1��д���������������Һ��Ӧ�ķ���ʽ���Ƚ����ף�
��2���۲�ͼ�����ѷ�����Һ��pH�����������մ���7��˵���������������еμ�ǿ�����ơ�
��3����������Һ������Ϊagʱ����Һ�����ԣ���������ΪNaCl��HCl��
��4��ֻҪѧ��������pH����Һ���ȵĹ�ϵ�Լ���̪��Һ�ڼ�����Һ�������ֵ���ɫ�������ѡ���������Һ������Ϊbgʱ����Һ�Լ��ԣ����Եμӷ�̪����Һ�Ժ�ɫ��
�����Ѷȣ���
5������� ��ҵ���ɻ�ͭ����Ҫ�ɷ�CuFeS2��ұ��ͭ����Ҫ�������£�

��1������A�еĴ�����Ⱦ���ѡ�������Լ��е�______���գ�
A��ŨH2SO4��B������ˮ������C��NaOH��Һ����?D��ϡHNO3
��2����ϡH2SO4��������B��ȡ����������Һ���μ�KSCN��Һ��ʺ�ɫ��������Һ�л�����Fe2+�ķ�����______��ע���Լ�������
��3������ͭұ����ͭ�Ļ�ѧ��Ӧ����ʽΪ______��
��4����CuSO4��ҺΪ�������Һ���д�ͭ����Al��Zn��Ag��Pt��Au�����ʣ��ĵ�⾫��������˵����ȷ����______��
a����ͭ�ӵ�Դ����������������Ӧ������������������?b����Һ��Cu2+�������ƶ�
c������������ɻ���Ag��Pt��Au�Ƚ�������?d������ȫ��ת��Ϊ��ѧ��
��5�����÷�Ӧ2Cu+H2O2+H2SO4�TCuSO4+2H2O���Ƶ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������缫��ӦʽΪ______��
�ο��𰸣���1��������ͼת����֪������A�еĴ�����Ⱦ����Ҫ�Ƕ�������ѡ���Լ����ն��������ܲ����µ���Ⱦ���壬
a��ŨH2SO4�������ն�������a����
b����ˮ���������Ӧ����������泥���b��ȷ��
c��NaOH��Һ���������Ӧ�����������ƣ���c��ȷ��
d��ϡHNO3�������ն�����������NO��Ⱦ��������d����
�ʴ�Ϊ��bc��
��2����ϡH2SO4��������B��ȡ����������Һ���μ�KSCN��Һ��ʺ�ɫ��˵������Fe3+��Fe2+���л�ԭ�ԣ���������KMnO4��Һ���飬ȡ������Һ���μ�KMnO4��Һ��KMnO4��Һ��ɫ��ȥ��
�ʴ�Ϊ��ȡ������Һ���μ�KMnO4��Һ��KMnO4��Һ��ɫ��ȥ��
��3��������ͼת����֪��Cu2O��Al��Ӧ�û���Ӧ����Al2O3��Cu����Ӧ����ʽΪ3Cu2O+2Al?����?.?Al2O3+6Cu��
�ʴ�Ϊ��3Cu2O+2Al?����?.?Al2O3+6Cu��
��4��a������ͭʱ����ͭ�����������ӵ�Դ����������������Ӧ��a��ȷ����������������?
b����Һ��Cu2+�������ƶ�����b����
c��Ag��Pt��Au����ͭ���ã�ͭ�ŵ��Ag��Pt��Au�Ӵ�ͭ���䣬����������ɻ���Ag��Pt��Au�Ƚ�������c��ȷ����?
d����Ӧ�������ܲ��������Ե��ܲ���ȫ��ת��Ϊ��ѧ�ܣ���d����
�ʴ�Ϊ��ac��
��5�����÷�Ӧ2Cu+H2O2+H2SO4�TCuSO4+2H2O���Ƶ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������ǹ�������õ����ӷ�����ԭ��Ӧ��������Һ����ˮ����ʽ���ڣ��������缫��ӦʽΪ��2H++H2O2+2e-=2H2O���ʴ�Ϊ��2H++H2O2+2e-=2H2O��
���������
�����Ѷȣ�һ��