微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有甲、乙两个容积相等的恒容密闭容器,向甲容器中通入6molA和2molB,向乙容器中通入1.5molA、
0.5molB和3molC,保持两容器的温度恒定,使反应3A(g)+B(g)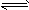 xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2。
xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2。
(1)若x=2,则平衡时甲、乙两容器A的物质的量_________(填“相等”或“不相等),此时甲中A的体积分数为___________,甲、乙两容器中的压强之比为___________。
(2)若x=4,平衡时甲、乙两容器中的压强之比为__________。
(3)若x=4,平衡后向甲容器中再加3molA和1molB,C的体积分数___________(填“大于”、“小于”或“等于”)0.2。
参考答案:(1)相等;0.6;1:1
(2)8:5
(3)等于
本题解析:
本题难度:一般
2、选择题 一定条件下,某容积不变的密闭容器内存在下列平衡:2HI(g) H2(g)+I2(g);则下列有关说法正确的是(?)
H2(g)+I2(g);则下列有关说法正确的是(?)
A.如仅仅改变浓度这一条件,使得体系颜色加深,则上述平衡在条件改变之后的移动方向无法判断:即可以正移或逆移,还可以不移动
B.如改变体系温度,体系颜色一定发生变化
C.继续充入HI气体,则HI的转化率将减小
D.温度不变时,当体系颜色变浅,则正反应速率和逆反应速率都将减小
参考答案:AB
本题解析:颜色的深浅和单质碘的浓度大小有关系,又因为该反应是体积不变的,所以A正确;任何化学反应都会伴随着能量的变化,因此改变温度平衡状态一定发生移动,B正确;由于体积不变,所以在加入HI气体相当于是增大压强,平衡是不变的,因此转化率不变,C不正确;颜色变浅,只能说明单质碘的浓度减小了,但反应速率不一定是减小的,D不正确,答案选AB。
点评:该题在解答时需要注意的是颜色的深浅和平衡是否移动及移动的方向是没有关系的,单质碘的浓度只要增大,颜色就会变深,而只要正逆反应速率不相等,平衡状态就会发生变化,所以必须灵活运用勒夏特例原理。
本题难度:一般
3、选择题 X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X+2Y 2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为? ( )
2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为? ( )
A.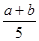 ×100%
×100%
B.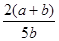 ×100%
×100%
C.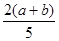 ×100%
×100%
D. ×100%
×100%
参考答案:B
本题解析:方法一:某反应物的转化率(α)= ?×100%,Y的起始物质的量为bmol,所以计算结果的分母中一定含有b,故选B;
?×100%,Y的起始物质的量为bmol,所以计算结果的分母中一定含有b,故选B;
方法二:利用三段式法计算:
X(g)? +? 2Y(g)? ? 2Z(g)
? 2Z(g)
起始:amol?bmol?0
转化:xmol? 2xmol? 2xmol
平衡:(a-x)mol?(b-2x)mol?2xmol
所以(a-x)mol+(b-2x)=2xmol
解得x=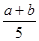 mol
mol
所以Y的转化率为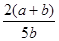 ×100%,故选B。
×100%,故选B。
本题难度:一般
4、选择题 在一定条件下,在体积为2L的密闭容器中发生反应:mA?+?nB=pC。t秒末,A减少了1?mol,B减少了1.25?mol,C增加了0.25?mol/L。则m?∶?n?∶?p应为
A.4∶ 5∶ 2?
B.2∶ 5∶ 4 ?
C.1∶ 3∶ 2?
D.3∶ 2∶ 1
参考答案:A
本题解析:物质的变化量之比是相应的化学计量数之比,所以m ∶ n ∶ p=4∶ 5∶ 2,答案选A。
本题难度:一般
5、填空题 右图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t是达到平衡状态的时间。试回答:
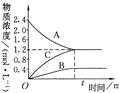
(1)该反应的反应物是?。
(2)该反应的化学方程式是:?。
(3)若达到平衡状态的时间为2min,则A的平均速率是?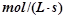 。
。
参考答案:(1)A?(2)3A 3C + B? (3)0.01
3C + B? (3)0.01
本题解析:(1)根据图像可知,A物质的浓度降低,所以A物质是反应物。
(2)平衡时A的浓度减少了2.4mol/L-1.2mol/L=1.2mol/L,B和C的浓度分别增加了0.4mol? /L和
1.2mol/L,则根据浓度的变化量之比是相应的化学计量数之比可知,反应的化学方程式是3A 3C + B。
3C + B。
(3)反应速率通常用单位时间内浓度的变化量来表示,则A的平均速率是1.2mol/L÷2min=0.6mol/(L・min)。
点评:该题是中等难度的试题,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生答题能力的培养。有利于调动学生的学习兴趣,提高学生应试能力和学习效率。该题的关键是在明确图像中曲线变化的基础上,灵活运用即可。
本题难度:一般