微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下列反应在210℃达到平衡:
PCl5(g) PCl3(g)+Cl2(g)?△H>0? K=1?①
PCl3(g)+Cl2(g)?△H>0? K=1?①
CO(g)+Cl2(g) COCl2(g)?△H <0? K=5×104?②
COCl2(g)?△H <0? K=5×104?②
COCl2(g) CO(g)+ Cl2(g)?△H>0?③
CO(g)+ Cl2(g)?△H>0?③
(1)化学平衡常数K表示可逆反应的进行程度,K值大小与温度的关系是:温度升高,K值_______?___________(填一定增大、一定减小、或可能增大也可能减小)。
(2)根据反应①的平衡常数K的表达式,平衡时,下列等式必定成立的是?
A.c(PCl5) = c(PCl3)= c(Cl2)="1?" B.c(PCl5)= c(PCl3)・c(Cl2)="1?" C.c(PCl5)= c(PCl3)・c(Cl2)
反应②和反应③的K值表达式?(填“相同”或“不同”)
(3)降低Cl2浓度,反应③的K值? ____?(填“增大”、“减少”或“不变”)。
参考答案:(1)?可能增大也可能减小
(2)C?不同?
(3)不变
本题解析:略
本题难度:简单
2、计算题 (6分)(1)某温度下,在一密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。分析有关数据,写出X、Y、Z反应的化学方程式?。
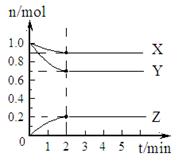
(2)某温度下,在另一密闭容器中充入2molX和3molY,然后按(1)中的化学方程式进行反应,当达到化学平衡时,测得Z的物质的量分数为25%,求平衡时X的转化率。
参考答案:(1)X+3Y 2Z (用“=”不给分)(2分)
2Z (用“=”不给分)(2分)
(2)? X? +? 3Y 2Z
2Z
起始量(mol)? 2? 3? 0
转化量(mol)? a? 3a? 2a
平衡量(mol)? 2-a? 3-3a? 2a
所以有
解得a=0.5
所以其转化率是 =25%。
=25%。
本题解析:(1)根据图像可知X和Y是反应物,Z是生成物,反应进行到2min是各种物质的物质的量不再发生变化,X、Y。Z物质的量的变化量分别为0.1mol、0.3mol、0.2mol,所以方程式为X+3Y 2Z。
2Z。
(2)可采用三段式进行计算。
本题难度:一般
3、选择题 A、B两种物质当浓度恒定时,在不同温度下进行反应:A +3B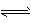 3C。10℃时,反应速率v(B) =0.3 mol.(L.s)-1; 50℃时,反应速率v(A) =25.6 mol.(L.s)-1。若该反应温度每升高10℃,化学反应速率增至n倍,则n值为
3C。10℃时,反应速率v(B) =0.3 mol.(L.s)-1; 50℃时,反应速率v(A) =25.6 mol.(L.s)-1。若该反应温度每升高10℃,化学反应速率增至n倍,则n值为
[? ]
A.4
B.3
C.3.5
D.2.5
参考答案:A
本题解析:
本题难度:一般
4、实验题 以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程如下:
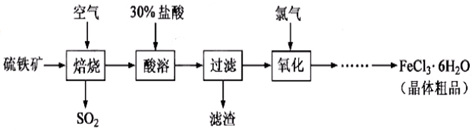
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g) 2SO3(g) ,该反应的平衡常数表达式为K= ??;过量的SO2与NaOH溶液反应的化学方程式为?
2SO3(g) ,该反应的平衡常数表达式为K= ??;过量的SO2与NaOH溶液反应的化学方程式为?
(2)酸溶及后续过程中均需保持盐酸过量,其目的是?、??。
(3)通氯气氧化后时,发生的主要反应的离子方程式为??;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 ?(写化学式)。
参考答案:(1)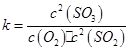 ? SO2+NaOH=NaHSO3;
? SO2+NaOH=NaHSO3;
(2)提高铁元素的浸出率?抑制Fe3+水解
(3)Cl2+2Fe2+=2Cl-+2Fe3+? Cl2? HCl
本题解析:(1)根据化学平衡常数概念写出平衡常数表达式;在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g) 2SO3(g) ,该反应的平衡常数表达式为
2SO3(g) ,该反应的平衡常数表达式为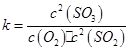 ;过量的SO2与NaOH溶液反应生成亚硫酸氢钠,化学方程式为SO2+NaOH=NaHSO3;(2)根据题给流程知,酸溶的目的是将氧化铁转化为氯化铁,盐酸可抑制铁离子水解,酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、抑制Fe3+水解。(3)通氯气氧化的目的是将亚铁离子氧化为铁离子,发生的主要反应的离子方程式为Cl2+2Fe2+=2Cl-+2Fe3+;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为Cl2、HCl。2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程为载体考查平衡常数表达式的书写、物质的分离和提纯。
;过量的SO2与NaOH溶液反应生成亚硫酸氢钠,化学方程式为SO2+NaOH=NaHSO3;(2)根据题给流程知,酸溶的目的是将氧化铁转化为氯化铁,盐酸可抑制铁离子水解,酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、抑制Fe3+水解。(3)通氯气氧化的目的是将亚铁离子氧化为铁离子,发生的主要反应的离子方程式为Cl2+2Fe2+=2Cl-+2Fe3+;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为Cl2、HCl。2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程为载体考查平衡常数表达式的书写、物质的分离和提纯。
本题难度:一般
5、计算题 在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
试求:
(1)NO2的转化率为?
(2)反应前后的压强比为多少?
(3)用O2来表示的反应速率是多少mol・L-1・min-1
参考答案:(1)80%
(2)P前/P后= 5/7
(3)0.024 mol・L-1・min-1
本题解析:
本题难度:一般