微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题
(8分)实验室制取气体常用的装置如下列图示,请回答下列问题:(选用装置时填字母编号)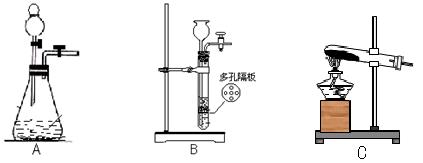 ?
?
(1)若实验室选用装置C制取氨气,则反应的化学方程式为
________________________________________ ______________________,
______________________,
检验NH3收 满的方法:____________________________________________________;
满的方法:____________________________________________________;
(2)若实验室利用过氧化钠与水反应制取氧气,则应选择__________装置,有关反应的化学方程式为:________________________________________________。
参考答案:

本题解析:略
本题难度:简单
2、实验题 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗产品并精制的流程:
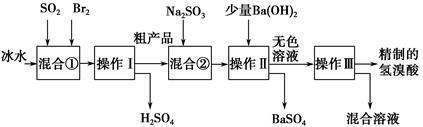
根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为________________________________。
(2)混合①中使用冰水的目的是_______________________________________。
(3)操作Ⅲ一般适用于分离________混合物。(填序号)
a.固体和液体? b.固体和固体
c.互不相溶的液体? d.互溶的液体
(4)混合②中加入Na2SO3的目的是____________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察到的现象为__________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有________________,其用于证明该假设所用的试剂为____________。
参考答案:(5)KSCN溶液 溶液变成红色 Br2 CCl4(其他合理也可)
本题解析:SO2与Br2在水中发生氧化还原反应,反应放热,为防止溴蒸发,用冰水降温。操作Ⅰ、Ⅲ均是蒸馏,操作Ⅱ是过滤。混合②中加入Na2SO3的目的是除去粗产品中未反应完的溴。检验Fe3+常用KSCN溶液;工业氢溴酸中可能含有溴而呈淡黄色,可用四氯化碳萃取而证明。
本题难度:困难
3、实验题 取wg含有杂质(杂质受热不分解)的NH4HCO3,选用如图所示的装置,制取一瓶干燥的氨气,多余氨气全部被水吸收。回答:
(1)选用的装置是(用A、B、C……回答)?,连接选取装置的正确顺序是(a,b,c……填写):?接?;?接?;?接?。
(2)E装置中所盛药品的名称是?,其作用是?。
(3)若选用B装置,连接时b口进气还是C口进气?,其原因是?。
(4)若收集到氨气VmL(标准状况),氨水的浓度为a mol/L,则碳酸氢铵的纯度为
?%(设NH4HCO3全部分解)。
参考答案:(1)? AEBD?,? a?接 f ; g 接 c ; b 接 e
(2)碱石灰?,吸收水和CO2?。
(3) C口?,?氨气密度小于空气?。(4)略
本题解析:略
本题难度:简单
4、实验题 已知氯气和氢氧化钠的反应条件不同,产物也不同,在实验室里可用如图所示装置制取氯酸钠次氯酸钠和探究氯水的性质。
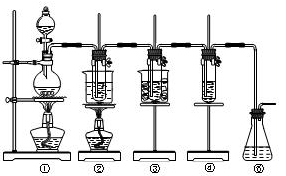
图中:①为氯气发生装置;②的试管里盛有15mL30%NaOH溶液,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_________(填写下列编号字母)的净化装置。
A.碱石灰
B.饱和食盐水
C.浓硫酸
D.饱和碳酸氢钠溶液