微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 I.(1)下列有关实验操作或测量数据合理的是___________(填写序号)
a.用铁坩埚加热CuSO4・5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8 mL的Na2CO3溶液
d.实验室酸制氯化亚锡溶液时,可以先将氯化亚锡溶解在盐酸中,再配制到所需要的浓度
e.使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤干净
f.在用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜以加快化学反应速率
II.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计如图所示实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题。

(2)实验室制备乙烯的化学方程式______________________。升温到140℃时的副反应产物的结构简式
___________。
(3)图中①.②.③.④装置可盛放的试剂是:①___________;②___________;③___________;
④___________。(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(4)能说明二氧化硫气体存在的现象是______________________
(5)使用装置②的目的是_________________________________
(6)使用装置③的目的是_________________________________
(7)确定含有乙烯的现象是_______________________________
参考答案:(1)cdf
(2)CH3CH2OH CH2=CH2↑+H2O;CH3CH2-O-CH2CH3
CH2=CH2↑+H2O;CH3CH2-O-CH2CH3
(3)① A ;② B ;③ A ;④ D 。
(4)装置①中品红溶液褪色
(5)除掉二氧化硫以免干扰乙烯的性质实验
(6)检验二氧化硫是否除尽
(7)③中的溶液褪色,④中的溶液不褪色
本题解析:
本题难度:一般
2、实验题 镁及其合金是用途广泛的金属材料,目前世界上60%的镁是从海水中提取的。.某学校课外兴趣小组从海水晒盐后的盐卤(主要含 等)中模拟工业生产来提取镁,主要过程如下,回答下列问题:
等)中模拟工业生产来提取镁,主要过程如下,回答下列问题:
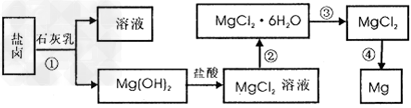
(1)从转化①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有_________的烧杯中,充分搅拌后经_________、_________(填操作方法)干燥可得纯净的Mg(OH)2,在此操作过程中,玻璃棒的作用是搅拌和__________
(2)写出转化④中发生反应的化学方程式__________________
(3)已知转化③的反应原理与制取无水AlCl3相同,下图是制取无水AlCl3实验装置图。装置A中的两液体分别是浓硫酸和浓盐酸。请回答:

①为什么不直接用加热方法来制取无水AlCl3,请用化学方式表示:_________;
②分液漏斗中应盛装的试剂是_________;
③由分液漏斗向烧瓶中加试剂时应注意的事项是_________
(4)含有铝元素的另一物质明矾作为膨化剂炸油条(饼)或膨化食品时,若在面粉里加入小苏打后,再加入明矾,则会使等量的小苏打释放出比单放小苏打多一倍的二氧化碳,这样就可以使油条(饼)在热油锅中一下子就鼓起来,得到香脆可口的油条(饼)了。请用化学反应方程式解释得到香脆可口的油条(饼)的原因:_____________________。
参考答案:(1)饱和MgCl2(或氯化镁)溶液;过滤;洗涤;引流
(2)MgCl2 Mg+Cl2↑
Mg+Cl2↑
(3)①?AlCl3+3H2O=Al(OH)3+3HCl↑(写成AlCl3+3H2O==Al(OH)3+3HCl↑、2?Al(OH)3==Al2O3+3H2O或写成2AlCl3+3H2O==Al2O3+6HCl↑也可以);②?浓盐酸;③控制分液漏斗活塞,使浓盐酸缓缓加入到浓硫酸中
(4)Al3++3HCO3-=?Al(OH)3↓+3CO2↑
本题解析:
本题难度:一般
3、选择题 下列试验现象预测正确的是
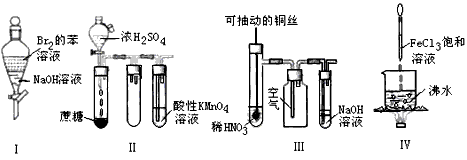
[? ]
A、实验I:振荡后静置,上层溶液颜色保持不变
B、实验II:酸性KMnO4溶液中出现气泡,溶液颜色不变
C、实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D、实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
参考答案:D
本题解析:
本题难度:一般
4、实验题 有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,进行了以下实验。
(1)检验矿物样品中是否有Fe3+
实验用品:锤子、研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
实验步骤: ①取样:将样品用锤子敲碎,再在研钵中研细备用。
②溶解:将样品粉末倒入烧杯,加入___________,用玻璃棒充分搅拌。
③?___________(填操作名称)。
④检验:取少许溶液,___________。实验现象:____________。
实验结论:矿物样品中含有Fe3+。
(2)制备氢氧化亚铁
①为了得到亚铁盐的溶液,同学们在剩余的溶液中加入过量的某种固体试剂,该试剂是(填化学式)__________,反应的离子方程式是?____________?。
②对于①中过量的的固体试剂是否需要除去,同学们产生了两种观点。
甲组:认为需要过滤。?
乙组:认为不需要过滤。
你支持的是组_________(填“甲”或“乙”),理由是?____________。
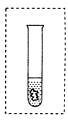
③同学们在新制得的亚铁盐溶液中加入适量新制的氢氧化钠溶液,制出的氢氧化亚铁呈__________色。为使试管中的氢氧化亚铁保存的时间更长,请在图中画出你的设计(可以加必要的文字说明)。
参考答案:(1)稀盐酸(其他合理答案也可);?过滤;?滴加KSCN溶液;?溶液变为红色?
(2)①?Fe?;?2Fe3+ +Fe=3Fe2+?
②?乙?;过量的铁粉可以防止Fe2+被氧化为Fe3+;
③白;可覆盖一层植物油、苯等
本题解析:
本题难度:一般
5、实验题 碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有_______晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)含0.800?mol?NH3的水溶液质量为54.0?g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为____%。
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为: ?
①粗盐溶解;
②加入试剂至沉淀完全,煮沸;
③____________________;
④加入盐酸调pH;
⑤加入____________;
⑥过滤;
⑦灼烧,冷却,称重。
(4)上述步骤②中所加入的试剂为_______、______。
(5)上述步骤④中加盐酸调pH的目的是________________。
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下: ?
含0.1?mol?NH4HCO3的溶液中加入0.1?mol?NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH4HCO3与NaOH的反应可能为_____(写离子方程式);若无沉淀,则NH4HCO3与NaOH的反应可能为______(写离子方程式)。该实验方案有无不妥之处?若有,提出修正意见。
___________________________
参考答案:(1)(NH4)2CO3?
(2)92%
(3)过滤、碳酸氢铵?
(4)氢氧化钠、碳酸钠
(5)中和过量的氢氧化钠和碳酸钠?
(6)HCO3-+OH-→CO32-+H2O;NH4++OH-→NH3+H2O;需先煮沸,然后滴加氯化钙稀溶液
本题解析:
本题难度:一般