��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����������в������������ý�����ȷ����
| ʵ�����������
| ʵ�����
|
A
| �ֱ���2 mL 0.1 mol��L��1 CH3COOH��Һ��2 mL 0.1 mol��L��1 H3BO3��Һ�еμӵ�Ũ�ȵ�NaHCO3��Һ��ǰ�������ݲ�������������������
| ���ԣ�
CH3COOH �� H2CO3�� H3BO3
|
B
| ��Ũ�Ⱦ�Ϊ0.1 mol��L��1 NaCl ��NaI �����Һ�еμ�����AgNO3��Һ��������ɫ����
| �ܶȻ���
Ksp(AgCl)��Ksp(AgI)
|
C
| ����ˮ�Ҵ��м���ŨH2SO4�����ȣ�����������ͨ������KMnO4��Һ����ɫ��ȥ
| ֤����������ϩ
|
D
| ����������ˮ����NaI��Һ�У��ٵμ�CCl4�������ã���Һ��Ϊ���㣺�ϲ���Һ��ɫ���²���Һ�Ϻ�ɫ
| �����ԣ�Br2��I2
|
2������� С����ϲ����ѧʵ��Σ�����Ҫѧϰ��̽�������仯����������Ի�ԭ�ԡ���
��1��ʵ��ǰС��Ԥ��˵��Fe2+�϶����л�ԭ�����������ԣ�����Ϊ��Ԥ��������ǣ�______��
��2��С������ʵ��֤������Ԥ�⣮ʵ�����ṩ�������Լ���3%��H2O2��Һ��п����ͭƬ��0.1mol?L-1FeCl2��Һ��KSCN��Һ��������ˮ��
����С���ƻ���0.1mol?L-1FeCl2��Һ����������ˮ��̽��Fe2+�Ļ�ԭ�ԣ���Ԥ�ƿ��ܷ����ķ�Ӧ�ǣ�______д���ӷ���ʽ�������ܹ۲쵽�������ǣ���Һ��dz��ɫ��Ϊ______?ɫ��
��ʵ���У�С����������̫���ԣ���ʦ���������Dz���ĺ���̫�ͣ��������ͨ������Fe2+�������IJ���Fe3+�Ĵ����Ի�ȡ֤�ݣ�����Ϊ��ѡ______�������ƣ�����С�����õĻ��Һ�У���ͨ����Һ����______ɫ������֤��С���Ĺ۵��ʵ�鷽��������ȷ�ģ�
�۶���֤��Fe2+���������ԣ�С����Ϊ�������ʶ����л�ԭ�ԣ����ֱ�ͭƬ��п��Ͷ��FeCl2��Һ�У����ͭƬû�仯��п����С���ɴ�˵�����ֽ����Ļ�ԭ����ǿ������˳��Ϊ��______��
��3��С������H2O2����Ԫ����-1�ۣ��м�ۣ�����������ʣ�H2O2��FeCl2�ķ�Ӧʱ��Fe2+������������
������ΪС������������⣺��Fe2+�ڷ�Ӧ�б��ֳ�������Ӧת����______���������ţ���ͬ������Fe2+�ڷ�Ӧ�б��ֳ���ԭ��Ӧת����______��
��ʵ����Fe2+�Ļ�ԭ�Խ�ǿ��ʵ���ҵ�FeCl2��Һ�������������ʣ����ӵķ����ǣ�______����ط�Ӧ�����ӷ���ʽ��______��
3��ʵ���� ��15�֣�Ϊ��̽��H2O2��H2SO3��Br2�����Ե����ǿ�����������ʵ�飨�г���������ȥ������ش��������⣺
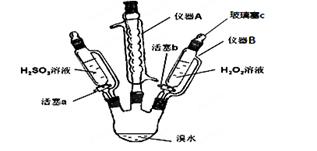
��1������A������_________����������___________��
��2��������B�μ�Һ�岢����Ҫ������c��ԭ����____________________________��
��3��ʵ���¼���£��벹ȫ�հף���
����
| ʵ�����
| ʵ������
| ʵ�����
|
��
| ����a����μ���H2SO3��Һ������
| ________________
| __________________________
|
��
| �����������Һ����μ���H2O2��Һ
| �տ�ʼ��Һ��ɫ�����Ա仯�������μӣ���Һ��Ϊ�Ȼ�ɫ
| __________________________
|
��4��������У���ʼʱ��ɫ�����Ա仯��ԭ���ǣ�д��һ����_______________________��
������з�Ӧ�����ӷ���ʽ_________________________________________________��
���������Ҫ��Ӧ�����ӷ���ʽ_____________________________________________��
4��ѡ���� ���ữ����MnSO4��Һ�еμ�(NH4)2S2O8(���������)��Һ�ᷢ����Ӧ��Mn2����S2O82-��H2O
5��ѡ���� X��Z��Y��W ��Ϊ���ֽ����� ����������ʵ����X+Y2+=X2++Y;��Z+2H2O(��ˮ)=Z(OH)2+H2��;��Z2+�������Ա�X2+��������Y��W�缫��ɵ�ԭ��أ��缫��ӦΪW2++2e��=W��Y��2e��=Y2+,��֪X��Y��Z��W�Ļ�ԭ����ǿ������˳��Ϊ? (? )
A��X��Z��Y��W
B��Z��W��X��Y
C��Z��Y��X��W
D��Z��X��Y��W