��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��13�֣���Щ�������������Ƶ�����ּ���������������̼�������������������ǵ��¼�����������Ҫ���أ��о���Щ��������ۺϴ���������Ҫ���塣
��1����ҵ�Ͽ����ö�����̼�Ͱ����ϳ����أ����ܷ�Ӧ���£�
2NH3(g)+CO2(g)  CO(NH2)2(l)+H2O(l)?
CO(NH2)2(l)+H2O(l)?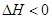 ���÷�Ӧ��?����ϸ��¶ȡ��ϵ��¶ȡ��������Է����С�
���÷�Ӧ��?����ϸ��¶ȡ��ϵ��¶ȡ��������Է����С�
��2����֪�ϳ����ط��������У�
��1����2NH3(g)+CO2(g) ?NH2COONH4(s)?
?NH2COONH4(s)?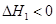
��2����NH2COONH4(s) ?CO(NH2)2(l)+ H2O(l)?
?CO(NH2)2(l)+ H2O(l)?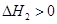
����ʾ��ͼ��[a��ʾ2NH3(g)+ CO2(g)��b��ʾNH2COONH4(S)��c��ʾCO(NH2)2(l)+ H2O(l)]������ȷ��ʾ���غϳɹ����������仯���ߵ��ǣ�����ţ�?��
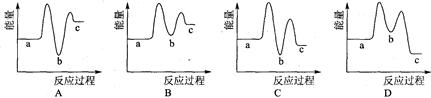
��3���ϳ����ع����У���NH3��CO2�����ʵ���֮��Ϊ1:2ʱ��NH3
��ת������ʱ��ı仯��ϵ��ͼ��ʾ��
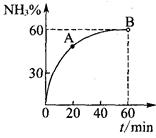
��A����淴Ӧ����v��(CO2) ?B����淴Ӧ����
v�� (CO2)(�������������=��)��
�ڴﵽƽ��ʱ��CO2��ת����Ϊ ?��
��4������̿�����ڴ���������Ⱦ��NO����ij1L�����ܱ������м���? 0.100molNO?��2.030mol�������̿�������ʣ�����������E������F�����¶ȷֱ���T1���T2��ʱ�����ƽ��ʱ�����ʵ����ʵ������±���
 ���� ����
n/mol
T/��
| ����̿
| NO
| E
| F
|
T1
| 2.000
| 0.040
| 0.030
| 0.030
|
T2
| 2.005
| 0.050
| 0.025
| 0.025
|
�������ϱ����ݣ�д��NO�����̿��Ӧ�Ļ�ѧ����ʽ?��
��������Ӧ��T1��ʱ��ƽ�ⳣ��ΪK1����T2��ʱ��ƽ�ⳣ��ΪK2������K1=?�����������Ϣ�жϣ�T1��T2�Ĺ�ϵ��?��
A. T1>T2? B. T1<T2? C.���Ƚ�?
�����ܱ�����Ϊ�ݻ��ɱ䣬���ݻ�ѧ��Ӧԭ������������ѹǿ�Ը÷�Ӧ��Ӱ��?
?��
2������� ��ˮ�ĵ���ƽ���У�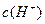 ��
��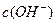 �Ĺ�ϵ����ͼ��ʾ��
�Ĺ�ϵ����ͼ��ʾ��
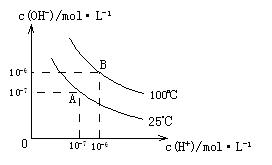
��1��A��ˮ�����ӻ�Ϊ1��10-14��B��ˮ�����ӻ�Ϊ?�����ˮ�����ӻ��仯��ԭ����?��
��2��25��ʱ��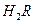 ��ˮ��Һ�еĵ��뷽��ʽΪ��
��ˮ��Һ�еĵ��뷽��ʽΪ��
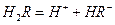 ��
��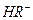

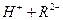 ��
��
�� 0.1 mol/L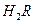 ��Һ��pH?1�����������������������
��Һ��pH?1�����������������������
����0.1 mol/L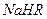 ��Һ�У�������Ũ���ɴ�С��˳���ǣ�
��Һ�У�������Ũ���ɴ�С��˳���ǣ�
?��
��3��100��ʱ��0.01 mol/L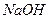 ��Һ��pH = ?��
��Һ��pH = ?��
��4��100��ʱ����pH =8��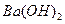 ��Һ��pH =5��ϡ�����ϣ�������100����£���ʹ�����Һ��pH =7����
��Һ��pH =5��ϡ�����ϣ�������100����£���ʹ�����Һ��pH =7����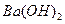 ��Һ������������Ϊ?��
��Һ������������Ϊ?��
3��ѡ���� ��һ�������£���2 mol X��3 mol Y����һ�ܱ������У��������¿��淴Ӧ��nX(g)��3Y(g)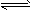 2Z(g)�ﵽƽ��ʱ��X��ת����Ϊa%��Y��ת����Ϊb%����a��b����n��ֵΪ
2Z(g)�ﵽƽ��ʱ��X��ת����Ϊa%��Y��ת����Ϊb%����a��b����n��ֵΪ
[? ]
A��1
B��2
C��3
D��4
4��ѡ���� ��2 L���ܱ������з�����ӦxA(g)��yB(g) zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����
zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����
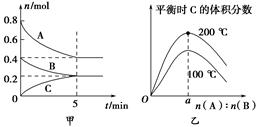
A��200 ��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 mol��L��1��min��1
B��200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25 L2/mol2
C�������������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D����ͼ�ҿ�֪����ӦxA(g)��yB(g) zC(g)�Ħ�H<0����a��2
zC(g)�Ħ�H<0����a��2
5������� �������ʵ�����A��B�����2L���ܱ������У��������з�Ӧ��3A(g)+B(g)=xC(g)+2D(g)����4min ���֪D��Ũ��Ϊ0. 5mol��L-1��CA��CB=3��5��C��ƽ����Ӧ������0.125mol��L-1��min-1����ʱA�����ʵ���Ũ��Ϊ___��B��ƽ����Ӧ����Ϊ___��xֵ��____��