��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �±���ϡ������ij������Ӧ��ʵ�����ݣ��������ݣ��ش��������⣺
| ʵ����� | ����
����/g | C��H2SO4��
/mol?L-1 | C��H2SO4��
/mol?L-1 | V��H2SO4��
/mL | ��Һ�¶�/�� | ������ʧ��ʱ��/s
��Ӧǰ
��Ӧ��
1
0.10
˿
0.5
50
20
34
500
2
0.10
��ĩ
0.5
50
20
35
50
3
0.10
˿
0.7
50
20
36
250
4
0.10
˿
0.8
50
20
35
200
5
0.10
��ĩ
0.8
50
20
36
25
6
0.10
˿
1.0
50
20
35
125
7
0.10
˿
1.0
50
35
50
50
|
��1��ʵ��4��5������______?�Է�Ӧ������Ӱ�죬______����Ӧ����Խ�죬�����ܱ���ͬһ���ɵ�ʵ�黹��______?����ʵ����ţ���
��2����������Ӧ��Ũ�ȶԷ�Ӧ���ʲ���Ӱ���ʵ����______����ʵ����ţ���
��3����ʵ����Ӱ�췴Ӧ���ʵ��������ػ���______����ʵ�������______��
��4��ʵ���е����з�Ӧ����Ӧǰ����Һ���¶ȱ仯ֵ��Լ15�棩������Ʋ���ԭ��______��
�ο��𰸣���1���Ա�ʵ��4��5����Ӧ���Ũ�Ⱥ�ʵ���¶���ͬ��������IJ�ͬ����ĩ״������Ӧ���ʴ̽�����ǹ��������Է�Ӧ���ʵ�Ӱ�죬����1��2ʵ��Ҳ�ܱ���ͬһ���ɣ��ʴ�Ϊ�����巴Ӧ��ı�����������Խ��?1��2��
��2����������˿���У�1��3��4��6�������Ƿ�ĩ���У�2��5���������У�����״̬��ͬ��Ũ�Ȳ�ͬ��������Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻
�ʴ�Ϊ��1��3��4��6?��2��5��
��3��6��7ʵ�����ı������ͬ����Ӧ���Ũ����ͬ������Ӧ���¶Ȳ�ͬ��̽�������¶ȶԷ�Ӧ���ʵ�Ӱ�죬
�ʴ�Ϊ����ʼ��Ӧ�¶ȣ�6��7��
��4���������еķ�Ӧ�У���������0.10g�����ᶼ��50ml��Ũ��Ҳ��һ����������ȫ��Ӧ����Ӧ�ų���������Ȼ��ȣ�
�ʴ�Ϊ��һ�����Ľ��������������ᷴӦ�ų���������ͬ��
���������
�����Ѷȣ�һ��
2��ѡ���� ������ϡ����ķ�Ӧ�У���֪10sĩ�����Ũ�ȼ�����0.6mol/L���������Ƿ�Ӧ��������Һ����ı仯����10s��������������ƽ����Ӧ�����ǣ�������
A��0.02mol/��L?min��
B��1.8mol/��L?min��
C��1.2mol/��L?min��
D��0.18mol/��L?min��
�ο��𰸣�10sĩ�����Ũ�ȼ�����0.6mol/L������v��H2SO4��=0.6mol/L10s=0.06mol/��L?s��=3.6mol/��L?min����
�������ᷢ����Ӧ2Al+3H2SO4�TAl2��SO4��3+3H2������������֮�ȵ��ڻ�ѧ������֮�ȣ�
����v[Al2��SO4��3]=13v��H2SO4��=13��3.6mol/��L?min��=1.2mol/��L?min����
��ѡC��
���������
�����Ѷȣ���
3������� ��һ���Ϊ10 L�������У�ͨ��һ������CO��H2O,850 ��ʱ������Ӧ��
CO(g)��H2O(g)  CO2(g)��H2(g)
CO2(g)��H2(g)
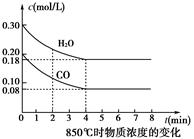
��1��CO��H2OŨ�ȱ仯��ͼ����0��4 min��ƽ����Ӧ����v(CO)��______mol��L��1��min��1��
��2����ͼ��4��5min֮��÷�Ӧ________(��ǡ���)����ƽ��״̬���ж�����________________________________________________________________________��
�ο��𰸣���1��0.03����2���ǡ���Ӧ���Ũ�Ȳ��ٱ仯
�����������1������ͼ���֪��0��4 min��COŨ�ȼ�����0.20mol/L��0.08mol/L��0.12mol/L��ƽ����Ӧ����v(CO)��0.12mol/L��4min��0.03 mol��L��1��min��1��
��2������ͼ���֪����Ӧ���е�4minʱ�������ʵ�Ũ�Ȳ��ٷ����仯����Ӧ�ﵽƽ��״̬����4��5min֮��÷�Ӧ�Ǵ���ƽ��״̬��
�����������ǻ���������Ŀ��飬�ѶȲ�����ȷ��Ӧ���ʵļ������ݺ�ƽ��״̬�������ǽ���Ĺؼ�������������ѧ������˼ά�����淶����������
�����Ѷȣ�һ��
4��ѡ���� ��һ�������£���ӦN2+3H2 2NH3��10L�ܱ������н��У����2min�ڣ�N2�����ʵ�����6mol���ٵ�2mol����2min��N2��ƽ����Ӧ����Ϊ��?��
2NH3��10L�ܱ������н��У����2min�ڣ�N2�����ʵ�����6mol���ٵ�2mol����2min��N2��ƽ����Ӧ����Ϊ��?��
A��0.4 mol/(L��min)
B��0.2 mol/(L��min)
C��0.3 mol/(L��min)��
D��0.6mol/(L��min)
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� Ϊ����ȡ�⣬��ͨ����Ӧ��2NO+O2==2NO2?NO2+2H+ +2I- ="=NO" + I2+H2O�Ƶã�NO���Ƶ�����е�������
A����ԭ��
B��������
C������
D����Ӧ��
�ο��𰸣�C
������������ݷ�Ӧ�۲��֪��Ӧǰ��NO�ĵ�����û�з����仯���������˻�ѧ��Ӧ��������������ã�����C��
�����Ѷȣ���