��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�¶��£��ֱ�ϡ�͵�pHֵ������ʹ��ᣬ��ҺpH�����ˮ������仯����������ͼ��ʾ����ͼ�ж�����˵����ȷ���ǣ�?��
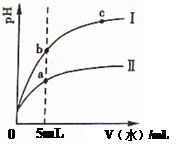
A����Ϊ����ϡ��ʱpH�仯����
B����Һ�ĵ����ԣ�b��a��c
C��ȡ��0�����������������Һ�ֱ���������ۣ��ų�H2�������������
D��ȡ5mL�������������Һ�ֱ�����ͬ��Zn����Ӧ����ʼʱ�ķ�Ӧ���ʣ���>��
�ο��𰸣�C
�����������ʼʱ���������pH��ȣ�����������δ����Ĵ��ᣬϡ�����л���벹��H+������ϡ����������pH�仯��A������Һ������������Ũ�Ⱥ�������������йأ�������a>b>c��B������ʼʱ����ʹ���pH��ȣ�n(CH3COOH)>n(HCl)�����������۷�Ӧ�ų���������࣬C��ȷ��5mLʱ��c(H+)�������п��Ӧ����죬D����
������ͬpHǿ�ᡢ����ϡ����ͬ������ǿ��pH�仯��ͬpHǿ�����ϡ����ͬ������ǿ��pH�仯��
�����Ѷȣ���
2��ѡ���� ��0.1mol?N2O4����1L�ܱ���ƿ�У�Ȼ����ƿ����100��ĺ��²ۣ���ƿ�ڵ�������Ϊ����ɫ��N2O4��g������ɫ���T2NO2��g��������ɫ�����н��۲���˵��������Ӧ�ڸ��������Ѿ��ﵽƽ��״̬���ǣ�������
A����ƿ���������ɫ���䣬���ټ���
B��N2O4������������NO2����������֮��Ϊ1��2
C��NO2������������NO2�������������
D��NO2�����ʵ���Ũ�Ȳ���
�ο��𰸣�A���÷�Ӧ�У�NO2Ϊ����ɫ���壬�������������ɫ���䣬˵��Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����A��ȷ��
B�������Ƿ�ﵽƽ��״̬��������N2O4������������NO2����������֮��Ϊ1��2������˵�����淴Ӧ������ȣ���B����
C��NO2������������NO2������������ȣ�˵�����淴Ӧ������ȣ��ﵽƽ��״̬����C��ȷ��
D��NO2�����ʵ���Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����D��ȷ��
��ѡB��
���������
�����Ѷȣ���
3������� ��15�֣�
A��B��C��D������ѧ��ѧ�еij���������������ڱ�ǰ18��Ԫ����ɣ�DΪ����ɫ���壬�ס����������ֵ��ʣ����ϵ��ʺͻ�����֮������ͼ1��ʾ�ķ�Ӧ��ϵ����Ӧ������������ʡ�ԣ���

��ش��������⣺
��1��ͼ1��ʾת�������а����ķ�Ӧ������?������ĸ����
a���û���Ӧ? b�����ֽⷴӦ? c���ֽⷴӦ? d�����Ϸ�Ӧ
��2��ͼ1�з�Ӧ�ٵĻ�ѧ����ʽ��?����3�֣�
��3��ͼ1�з�Ӧ����һ��������Ϊ���淴Ӧ����Ӧ�������仯��ͼ2��ʾ�����÷�Ӧ����ƽ��״̬ʱ�����д�ʩ�����������C��ƽ��ת���ʵ���?������ĸ����
A�������¶�? B�������¶�? C������ѹǿ
D����Сѹǿ? E���������? F������C����
��4������l.00 mol��2.00 mol C��ϳ����ݻ�Ϊ2 L���ܱ������У�3���Ӻ�Ӧ�ﵽƽ�⡣ƽ��������������ʵ���Ϊ2.55mol���üױ�ʾ�Ļ�ѧ��Ӧ����Ϊ
?mol?L-1?min-1��
��5���ݻ���Ϊ2 L���ĸ��ܱ������о������ţ�4���еķ�Ӧ��ij�¶��£����������ʵ�����mol�������淴Ӧ���ʹ�ϵ���±���ʾ��
�������
| n(��)
| n(C)
| n (D)
| v����v��Ĺ�ϵ
|
��
| 0.20
| 0.10
| 0.20
| v����v��
|
��
| 0.20
| 0.40
| 1.00
| ��?
|
��
| 0.60
| 1.20
| 0.80
| ��?
|
��������ʽϵ��Ϊ��������ȣ�����¶��µ�ƽ�ⳣ��K=?
��д���пո�?��??��?
�ο��𰸣���1�� c��d����1�֣�д��1����1�֣�����2��ֹ��
��2��4NH3+5O2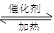 ?4NO + 6H2O��3�֣�
?4NO + 6H2O��3�֣�
(3)? B��C ����1�� ��д��1����1�֣�����2��ֹ��
(4)? 0.075��2�֣�
(5)?��40��2�֣�?�ڣ���2�֣�?�ۣ���2�֣�
���������DΪ����ɫ����,��D��NO2����˷�Ӧ����NO������������������ԭ��Ӧ��������������C��NO��������B��Ӧ������Ҳ��NO����˵��B�ǰ�������Ӧ�����ڰ��Ĵ���������A��H2O�����ˮ�õ���������������������������
��1���ڢ۷ֱ��ǷֽⷴӦ�ͻ��Ϸ�Ӧ������������ԭ��Ӧ��
��2�����������������ķ�ӦʽΪ4NH3+5O2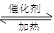 ?4NO + 6H2O
?4NO + 6H2O
��3����Ӧ�۵ķ�ӦʽΪ2NO��O2 2NO2������ͼ����жϣ���Ӧ�Ƿ��ȷ�Ӧ������Ҫ�ṩת���ʿ���ͨ�������¶ȣ�������ѹǿ���ṩת���ʡ���������Ӱ��ƽ��״̬��ת���ʲ��䣬����C�����ʵ�����ƽ��������Ӧ�����ƶ�����C��ת���ʻή�͡�
2NO2������ͼ����жϣ���Ӧ�Ƿ��ȷ�Ӧ������Ҫ�ṩת���ʿ���ͨ�������¶ȣ�������ѹǿ���ṩת���ʡ���������Ӱ��ƽ��״̬��ת���ʲ��䣬����C�����ʵ�����ƽ��������Ӧ�����ƶ�����C��ת���ʻή�͡�
��4��? 2NO��O2 2NO2
2NO2
��ʼ����mol��? 2? 1? 0
ת������mol��? 2x? x? 2x
ƽ������mol��? 2��2x 1��x? 2x
������2��2x��1��x��2x��2.55
���x��0.45mol
�����üױ�ʾ�Ļ�ѧ��Ӧ����Ϊ
��5�����淴Ӧ������ȣ�˵����Ӧ�ﵽƽ��״̬������ƽ�ⳣ��Ϊ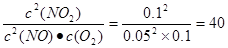 ���ڢ�
���ڢ�
 ��40����������Ӧ����С���淴Ӧ���ʡ��ڢ�
��40����������Ӧ����С���淴Ӧ���ʡ��ڢ�
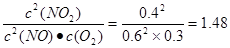 ��40����������Ӧ���ʴ����淴Ӧ���ʡ�
��40����������Ӧ���ʴ����淴Ӧ���ʡ�
�����Ѷȣ�һ��
4������� ��13�֣���1���������з�Ӧ��2SO2 + O2?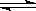 ?2SO3�����2min��SO2��Ũ����6 mol/L�½�Ϊ2 mol/L����ô����SO2Ũ�ȱ仯����ʾ�Ļ�ѧ��Ӧ����Ϊ____________����O2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ_____________��
?2SO3�����2min��SO2��Ũ����6 mol/L�½�Ϊ2 mol/L����ô����SO2Ũ�ȱ仯����ʾ�Ļ�ѧ��Ӧ����Ϊ____________����O2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ_____________��
��2����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2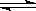 2SO3?��H<0?�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����
2SO3?��H<0?�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����

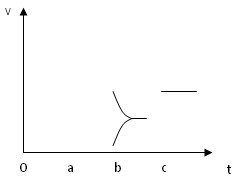
��a b�����иı������������?��
��b c�����иı������������?��
��������������뽫��Ӧ�ٶȱ仯�������c~d����
(3)���û�ѧƽ���ƶ�֪ʶ���;��õ���ˮ(�����dz��ڷ����ڼ����)�����dz����ɫ��ʧ����Һ���ϡ����:?
�ο��𰸣���1��2mol/(L��min)�� 1mol/(L��min)���������֣�������ֵ��û�֣�û��λ��һ�֣�
��2�����£���СSO3Ũ�ȣ�����һ�֣�
 ��ͼ1�֣�
��ͼ1�֣�
(3)����ˮ�д���ƽ��:Cl2+H2O 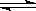 ?HCl + HClO ,HClO�����ֽ�ΪHCl��O2,ʹ��ƽ����ϵ��HClOŨ�ȼ�С,ƽ��������Ӧ�����ƶ�,Cl2Ũ�ȼ�С.HClŨ������,���dz��ɫ��ʧ,��Һ���ϡ����.��3�֣�
?HCl + HClO ,HClO�����ֽ�ΪHCl��O2,ʹ��ƽ����ϵ��HClOŨ�ȼ�С,ƽ��������Ӧ�����ƶ�,Cl2Ũ�ȼ�С.HClŨ������,���dz��ɫ��ʧ,��Һ���ϡ����.��3�֣�
�����������1���ԣ�SO2��=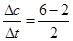 =2mol/(L��min)���ԣ�SO2��=
=2mol/(L��min)���ԣ�SO2��= ���ԣ�SO2��=1mol/(L��min)
���ԣ�SO2��=1mol/(L��min)
��2����a b���������淴Ӧ���ʾ�������ƽ�������ƶ���Ӧ��������
��b c�������淴Ӧ����˲���С��ƽ�������ƶ���Ӧ���Ǽ�С�˲���Ũ��
����������������淴Ӧ����ͬ��������
��3������
�����Ѷȣ�һ��
5��ѡ���� ���淴Ӧ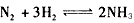 �������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯����ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����
�������淴Ӧ���ʿ��ø���Ӧ���������Ũ�ȵı仯����ʾ�����и���ϵ����˵����Ӧ�Ѵﵽƽ��״̬����
[? ]
A��3v��(N2) = v��(H2)
B��V��(N2)= v��(NH3)
C��2v��(H2) = 3v��(NH3)
D��v��(N2) = 3v��(H2)
�ο��𰸣�C
���������
�����Ѷȣ�һ��