��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���¶��£�������㶨Ϊ2 L���ܱ����������2 mol M��һ������N����������?��Ӧ��M(g)+N(g) E(g)������Ӧ���е�4minʱ�ﵽƽ�⣬���M��Ũ��Ϊ0��2 mol��L-1������˵����ȷ����
E(g)������Ӧ���е�4minʱ�ﵽƽ�⣬���M��Ũ��Ϊ0��2 mol��L-1������˵����ȷ����
A��4 minʱ��M��ת����Ϊ80��
B��4 minʱ����M��ʾ�ķ�Ӧ����Ϊ0��8 mol��L-1��min-1
C��4 min���������г��벻���뷴Ӧ��ϡ�����壬M�����ʵ�����С
D��2 minʱ��M�����ʵ���Ũ��Ϊ0��6 mol��L-1
2������� ��һ�ݻ��̶����ܱ������н��еķ�Ӧ��N2��g��+3H2��g���P2NH3��g�������ﵽƽ��״̬�ı�־��______
�ٵ�λʱ��������n?mol?N2��ͬʱ����2n?mol?NH3�ڰ������������백�ķֽ��������?����N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ1��3��2��״̬?��N2��H2��NH3Ũ�����?�ݶϿ�1��N��N����ͬʱ��6��N-H���γɢ��������ܶȲ��ٸı��״̬?��������ѹǿ���ٸı��״̬���������ƽ����Է����������ٸı��״̬�ᷴӦ�ų����������ڷ�Ӧ���յ�������
3��ѡ���� N2(g)+3H2(g) 2NH3(g) ��92.4 kJ������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������
2NH3(g) ��92.4 kJ������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������
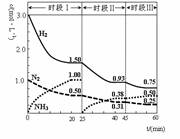
A��ǰ20���ӷ�Ӧ�ڷų�������Ϊ46.2kJ
B����25���Ӹı�������ǽ�NH3�ӷ�Ӧ��ϵ�з����ȥ
C������60����ʱ��Ӧ�ִﵽ��ƽ�⣬��ʱ��ı������������ѹǿ
D��ʱ�������ʼͶ�ŵ�����Ũ������ԭ����2������Ӧ���ת��������ƽ�ⳣ������
4������� ��һ��2L���ܱ������У�������Ӧ2SO3��g��?2SO2��g��+O2��g������H��0������SO3�ı仯��ͼ��ʾ��
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ______��
��2����O2��ʾ0��8min�ڸ÷�Ӧ��ƽ������v=______��
��3�������¶ȣ��÷�Ӧ�ķ�Ӧ���ʽ�______��Kֵ��______�������������ƽ����Է���������______�����������С�����䡱��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬����______
a��v��SO3��=2v��O2��?b��������ѹǿ���ֲ���? c��v�棨SO2��=2v����O2��? ?d���������ܶȱ��ֲ���
��5����8min��ѹ������Ϊ1L����SO3�ı仯����Ϊ______
A��?a?B��?b?C��?c?D��?d��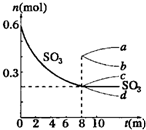
5������� ��6�֣���20L���ݵ��ܱ������У�����3mo1SO3(g)��lmo1��������һ���¶���ʹ�䷴Ӧ����Ӧ��4minʱ��������Ũ��Ϊ0.09 mol��L-1������Ӧ��8minʱ����Ӧ����ƽ�⣬��ʱ��������Ũ��c(SO3)=" a" mol��L-1��
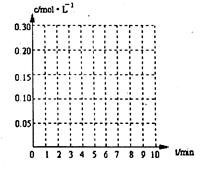
(1��0min��4min������O2ƽ������v(O2)= ?mol��L-1��min-1
(2)�ﵽƽ��ʱc(O2)=c(SO2)����a=?mol��L-1������������ϵ������0min��8min��֮��SO2��O2��SO3Ũ����ʱ��仯����.
(3)����ʼʱ���±�����Ͷ�ϣ���ͬ�¶��´ﵽƽ��ʱ����������Ũ�ȴ���a mol��L-1����?
?
| A
| B
| C
| D
|
SO3
| 1mol
| 3mol
| 3mol
| 0mol
|
SO2
| 2mol
| 1.5mol
| 0mol
| 6mol
|
O2
| 2mol
| 1mol
| 0mol
| 5mol
|