微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、
质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A.47
B.175
C.61
D.57
参考答案:D
本题解析:考查原子的组成及表示方法。在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和中子数之和是质量数所以该原子核内的中子数和质子数之差是293-118-118=57,答案选D。
本题难度:简单
2、实验题 (10分)某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
实验步骤
| 实验现象
|
1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液
| A. 浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色。
|
2.向新制得的Na2S溶液中滴加少量新制的氯水
| B.有气体产生,溶液变成浅红色
|
3.将一小块金属钠放入滴有酚酞溶液的冷水中
| C.剧烈反应,产生大量无色气体。
|
4.将镁条投入稀盐酸中
| D.反应不十分剧烈,产生无色气体
|
5.将铝条投入稀盐酸中
| E.生成淡黄色沉淀
|
请你帮助该同学整理并完成实验报告。
(1)实验目的:?。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等。
仪器:①?,试管,试管夹,烧杯,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(将与实验步骤对应的实验现象的编号和离子方程式填在答题卷上)
(4)实验结论:?。
参考答案:(1)探究同一周期主族元素性质的递变规律?(2)胶头滴管
(3)
实验内容
实验现象
离子方程式
1
B
?
2
E
S2-+Cl2=2Cl-+S↓
3
A
2Na+2H2O=2Na++2OH-+H2↑
4
C
?
5
D
?
本题解析:(1)根据实验步骤可知,该实验的目的是探究同一周期主族元素性质的递变规律。
(2)根据实验过程可知,实验中需要滴加液体,因此还需要胶头滴管。
(3)镁和冷水不反应,但在加热的条件下和沸水反应生成氢氧化镁和氢气,因此对应的现象是B。氯的非金属性强于硫的,因此氯水能把硫化钠中的硫离子氧化生成单质硫,现象是E。钠是活泼的金属,和水反应剧烈,现象是A。镁和铝都是活泼的金属,和盐酸反应生成生成氢气。但镁的活泼性强于铝的,所以镁反应更剧烈,现象分别是C、D。
(4)根据实验现象可知,同一周期主族元素从左到右失电子能力减弱,得电子能力增强,单质的还原性逐渐减弱,氧化性逐渐增强。
本题难度:一般
3、填空题 以下是一些元素的信息,其中有一种元素不在短周期。根据信息完成问题:
元素A
| 元素B
| 元素C
| 元素X
| 元素Y
| 元素Z
|
单质是一种常见金属,与元素X形成黑色和砖红色两种化合物
| 单质是一种黄绿色气体
| 短周期中金属性最强,与X反应能生成两种化合物
| 最外层电子数是内层电子数的3倍,能形成双原子阴离子
| 单质为双原子分子,结构中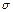 键与 键与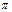 键数目比为1:2 键数目比为1:2
| 阳离子就是一个质子
|
?(1)写出A元素基态原子的核外电子排布式?。
(2)B、C、X的简单离子半径由大到小的顺序为?(用元素离子符号表示)。
(3)化合物YZ4B化学键的类型是?,检验该固体化合?物中阳离子的实验的方法和现象是?。
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程 ?。
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5mol・L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH=?(假设电解前后溶液体积不变)。
参考答案:
(1)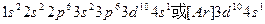 ? 2分
? 2分
(2)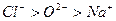 ? 2分
? 2分
(3)①离子键和共价键(说明:可不答配位健)? 2分
②取少量固体于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝? 3分
(4)2Cu+O2+CO2+H2O?Cu2(OH)2CO3 ? 3分
(5)12
本题解析:略
本题难度:一般
4、选择题 有A、B、C、D四种主族元素,A、B元素的阳离子和C、D元素的阴离子都具有相 同的电子层结构,且A的阳离子氧化性比B的阳离子氧化性弱,C的阴离子所带负电荷比D的阴离子所带负电荷多,则A、B、C、D的原子序数大小关系是(?)D
同的电子层结构,且A的阳离子氧化性比B的阳离子氧化性弱,C的阴离子所带负电荷比D的阴离子所带负电荷多,则A、B、C、D的原子序数大小关系是(?)D
A.B>A>C>D?B.C>B>A>D? C.A>B>C>D? D.B>A>D>C
参考答案:D
本题解析:略
本题难度:简单
5、选择题 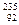 U是制造原
U是制造原 子弹的材料。
子弹的材料。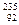 U的原子核内的中子数与核外电子数之差是
U的原子核内的中子数与核外电子数之差是
A ?235?B ?143?C ?92? D 51
参考答案:D
本题解析:略
本题难度:一般