微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.L层上的电子数为奇数的原子一定是主族元素的原子
B.元素周期表共有18列,第8列属于第ⅧB族、第17列属于第VIIA族
C.化学键的形成一定伴随着电子的转移和能量变化
D.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素
2、填空题 (10分)A、B、C、D、E、F都是短周期元素,原子序数依次增大。
元素
| 有关信息
|
A
| 原子最外层电子数和电子层数相等
|
B
| 原子的最外层电子数是内层电子数的2倍
|
C
| 元素主要化合价为-2,原子半径为66pm
|
D
| 与A同主族,最高价氧化物对应的水化物易溶于水
|
E
| 原子半径为104pm,所在主族序数与所在周期序数之差为3
|
F
| 单质为有色的气体
|
? (1)D2C的电子式?;
(2)沸点:A2C?A2E(填“>”或“<”或“=”);
(3)E的非金属性比F ?(填“强”或“弱”),并用化学事实加以说明(用化学方程式表示)?;
(4)化合物甲由A、B、C、D四种元素组成,其化学式量为84,是焙制糕点所用发酵粉的主要成分之一。写出甲在水溶液中与盐酸反应的离子方程式??。
3、选择题 有四组同族元素的物质,在101.3KPa时测定它们的沸点(0C)如下表所示:
第一组?
| He? -268.8?
| (a)? -249.5?
| ?Ar? -185.8?
| Kr? -151.7?
|
第二组?
| F2? -187.0?
| Cl2?-33.6?
| ?(b)? 58.7?
| I2? 184.0
|
第三组
| (c)? 19.4?
| ?HCl? -84.0
| ?HBr? -67.0?
| HI? -35.3
|
第四组
| H2O? 100.0?
| ?H2S? -60.2
| (d)? -42.0?
| H2Te? -1.8
|
?
下列各项中正确的是
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第二组物质只表现氧化性,不表现还原性
C.第三组物质中C的沸点最高,是因为c分子量最大
D.第四组中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te
4、选择题 放射性同位素铀 的原子核内的中子数是
的原子核内的中子数是
A.143
B.92
C.51
D.235
5、简答题 (12分)W、X、Y、Z是原子序数依次增大的短周期元素,它们中的两种或三种元素组成化合物甲、乙、丙、丁,几种物质的转化关系如图I所示。常温下0.01mol/L-1丙溶液
PH=12;XY2分子是非极性分子,但科学家在特殊条件下制得了XY2的原子晶体,其晶胞结构如图II所示。请回答下列问题:
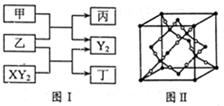
(1)甲与乙反应的化学方程式是______。
(2)甲的中心原子杂化轨道类型为_____;
XY2分子中,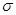 键与π键的数目之比为_________;
键与π键的数目之比为_________;
XY2原子晶体的1个晶胞中含有_______个原子。
W、X、Y、Z四种元素电负性由大到小的顺序是_______(用元素符号表示)。
工业上用氯气与潮湿的丁反应制备次氯酸的酸酐(棕黄色气体),同时生成小苏打和食盐混合物,反应的化学方程式是______________________________。