微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 取11.2 g铁粉和4.8 g硫粉均匀混合加热至红热,冷却后加足量盐酸,在标准状况下能收集到的气体体积为(? )
A.4.48 L
B.3.36 L
C.2.24 L
D.1.12 L
参考答案:A
本题解析:11.2 g铁粉即为0.2 mol,4.8 g S即为0.15 mol,根据Fe+S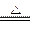 FeS可以判断Fe过剩,因此,将反应后所得物质与盐酸反应收集到的气体,既有FeS与盐酸反应生成的H2S,又有剩余的Fe与盐酸反应生成的H2。根据反应FeS+2HCl====FeCl2+H2S↑和Fe+2HCl====FeCl2+H2↑,可知最后所得气体的物质的量只与最初的铁粉的量有关,而与硫粉的量无关,即0.2 mol Fe发生反应可生成0.2 mol气体。
FeS可以判断Fe过剩,因此,将反应后所得物质与盐酸反应收集到的气体,既有FeS与盐酸反应生成的H2S,又有剩余的Fe与盐酸反应生成的H2。根据反应FeS+2HCl====FeCl2+H2S↑和Fe+2HCl====FeCl2+H2↑,可知最后所得气体的物质的量只与最初的铁粉的量有关,而与硫粉的量无关,即0.2 mol Fe发生反应可生成0.2 mol气体。
本题难度:简单
2、选择题 A(盐)和B(酸)反应,可放出有气味的气体C,C跟KOH反应又得到A(盐),C氧化的最终产物为W气,W气溶于水又得到B(酸)是(? )
A.K2S和稀H2SO4
B.K2SO3和盐酸
C.K2S和盐酸
D.K2SO3和稀H2SO4
参考答案:AD
本题解析:A项,K2S+H2SO4 H2S+K2SO4,H2S+2KOH
H2S+K2SO4,H2S+2KOH K2S+2H2O,2H2S+3O2
K2S+2H2O,2H2S+3O2 2SO2+2H2O,2SO2+O2
2SO2+2H2O,2SO2+O2 2SO3,SO3+H2O
2SO3,SO3+H2O H2SO4。D项,K2SO3+H2SO4
H2SO4。D项,K2SO3+H2SO4 K2SO4+H2O+SO2,SO2+2KOH
K2SO4+H2O+SO2,SO2+2KOH K2SO3+H2O,2SO2+O2
K2SO3+H2O,2SO2+O2 2SO3,SO3+H2O
2SO3,SO3+H2O H2SO4。
H2SO4。
本题难度:简单
3、选择题 下列说法不正确的是( )
A.硫是一种淡黄色的能溶于水的晶体
B.硫的化合物常存在于火山喷出的气体中和矿泉水里
C.硫在空气中燃烧的产物是二氧化硫
D.硫在纯氧中燃烧的产物是三氧化硫
参考答案:AD
本题解析:硫是一种淡黄色的晶体,但不溶于水,A不正确;S在空气中或纯氧中燃烧生成物都是二氧化硫,D不正确,答案选AD。
点评:该题是基础性试题的考查,试题基础性强,侧重对学生基础知识的巩固与训练,难度不大。该题的关键是熟练记住S的性质,并能灵活运用即可。
本题难度:一般
4、选择题 在某BaCl2溶液中通入SO2气体,未见沉淀生成;若先通入SO2气体,再通入另一种气体,则可看到沉淀生成;这种气体不可能是
A.Cl2
B.NH3
C.HCl
D.SO3(气体)
参考答案:C
本题解析:C、SO2和HCl气体分别通入BaCl2溶液,不发生化学反应,则观察不到沉淀生成,故错误。故选C。
点评:本题考查二氧化硫的性质,明确二氧化硫的还原性、酸性氧化物是解答本题的关键,题目难度不大。
本题难度:简单
5、填空题 (14分)已知:①FeS不溶解于水;②实验室制取H2S、SO2气体的原理是:
FeS+H2SO4=FeSO4+H2S↑? Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
③硫化氢与二氧化硫气体相遇会发生反应:2H2S+SO2=3S+2H2O
根据下图中A~D的实验装置和试剂进行实验,回答下列问题:

⑴装置A是由双孔塞、玻璃导管及?和?组装起来的
⑵组装一套制取SO2气体的装置,并证明SO2既有氧化性、又有还原性和漂白性
①按实验装置连接顺序,把a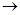 f各导管口连接起来,正确的顺序有?
f各导管口连接起来,正确的顺序有?
A.befcda
B.adcefb
C.acdfeb
D.acdefb