微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:FeSO4・7H2O)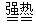 Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是
Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是
A.有BaSO4生成
B.有BaSO3生成
C.同时有BaSO4和BaSO3生成
D.有SO3逸出
2、实验题 (12分)根据下图回答问题:
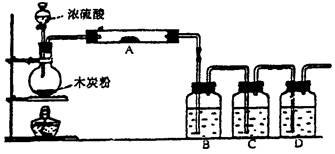
(1)写出浓H2SO4和木炭粉在加热条件下反应的化学方程式?。
(2)若用图中的装置检验上述反应的全部产物,完成下列各题:
A中加入的试剂是?,作用是?
B中加入的试剂是?,作用是?
C中加入的试剂是?,作用是?
D中加入的试剂是?,作用是?
(3)实验时,C中应观察到的现象是:?
3、选择题 将一张浸湿了溴水的滤纸挂在SO2气体中,滤纸会由黄色变成白色,这主要是因为(?)
A.SO2漂白了滤纸
B.SO2与Br2化合生成了无色的物质
C.反应放热使溴挥发了
D.Br2被SO2还原成无色的Br-
4、填空题 (8分)已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNa HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。
HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。

试回答下列问题:
(1)写出a点反应的离子方程式_____。
(2)写出b点到c点反应的离子方程式_________。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为_________mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
5、计算题 向铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500mL,再加入足量锌粉,使之充分反应,收集到2.24L(标准状况)气体。过滤残留固体,干燥后称量,质量减轻了7.5g。
(1)求参加反应的锌粉的物质的量
(2)原硫酸的物质的量浓度。