|
高中化学知识点归纳《难溶电解质的溶解平衡》高频试题强化练习(2017年最新版)(一)
2017-03-05 15:39:47
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 (3分)下列说法不正确的是__________。
A.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的;
B.对于Al(OH)3(s)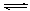 Al(OH)3(aq) Al(OH)3(aq) 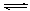 Al3++3OH-,前者为溶解平衡,后者为电离平衡; Al3++3OH-,前者为溶解平衡,后者为电离平衡;
C.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大
D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
|
2、选择题 已知:25 ℃时,CaCO3的Ksp=2.8×10-9,CaCO3在水中的溶解平衡曲线如图所示。下列说法正确的是
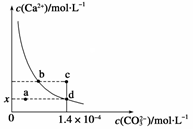
A.x数值为1.4×10-5
B.b点与d点对应的溶度积相等
C.加入蒸馏水可使溶液由d点变到a点
D.c点将有沉淀生成,平衡后溶液中c(Ca2+)、c(CO32-)一定相等
3、选择题 工业制氯化铜时,是将浓盐酸用蒸汽加热至80 ℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌使之溶解,反应如下:CuO+2HCl====CuCl2+H2O,FeO+2HCl====FeCl2+H2O。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀,pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。
为除去溶液中的Fe2+,可以采用的方法是(? )
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.通入适量Cl2,再加碱调整溶液的pH为4
D.直接加铁粉将Cu2+还原出来
4、选择题 下列实验操作对应的实验现象和解释或结论都正确的是
选项
| 实验操作
| 实验现象
| 解释或结论
| A
| 把S02通人紫色石蕊试液中
| 紫色褪去
| S02具有漂白性
| B
| 向NaOH溶液中滴加足量的MgCl2溶液,
然后再滴加足量的CuCl2溶液
| 先产生白色沉淀,然
后沉淀变蓝色
| 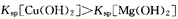
| C
| 向某溶液中滴加KSCN溶液
| 溶液变红色
| 溶液中含有Fe2+
| D
| 将充满N02的密闭玻璃球浸泡在热水中
| 红棕色变深
| 反应2NO2?N2O4的△H<0
|
5、选择题 已知常温下:Ksp〔Mg(OH)2〕=1.8×10-11,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12 ,
Ksp(CH3COOAg)=2.3×10-3。下列叙述正确的是
[? ]
A.等体积混合浓度均为0.2 mol・L-1的AgNO3溶液和CH3COONa溶液一定产生CH3COOAg沉淀
B.将0.001 mol・L-1的AgNO3溶液滴入0.001 mol・L-1的KCl和0.001 mol・L-1的K2CrO4溶液中,先产生Ag2CrO4沉淀
C.在Mg2+为0.121 mol・L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上
D.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大
|