��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��һ��С�ձ�����������⣬��һ�����������С�ձ��ϣ����ڱ������ϼ�������ˮ����С�ձ�����ʯ�����ϼ��ȣ��۲�ʵ������
��1�����ڱ������ϼ�������ˮ��������____________________________ ��
��2���۲쵽��ʵ��������______________________________________ ��
��3���ڱ��������ǵ��______________________________ ������塱�����Ǿ��塱����
��4�����ַ�����___________________________ ����ȡ����ķ�������_________________________ ��
�ο��𰸣���1����ȴ������
��2���ձ��г�����ɫ���������ڱ����������Ϻ�ɫ�ľ���
��3������
��4������������̬�������̡��ᾧ
���������
�����Ѷȣ�һ��
2��ʵ���� ij��ѧ�о���ѧϰС������ô�����ͭ������������������������������ʣ���ȡ��ˮ�Ȼ�ͭ���ⶨ��Ʒ������ͭ��������������ʵ��������ͼ��ʾ��
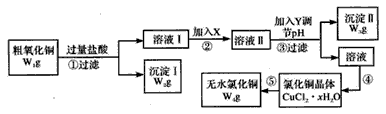
ʵ������е�pH����Ϊ��
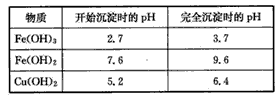
��ش��������⣺
(1)����١��۹��˲����У����õ�����������̨������Ȧ����©�����ձ��⣬����Ҫʹ�õ�������Ʒ��________��
(2)������з��������ӷ�Ӧ����ʽΪ________��____��
(3)�������ҺI�м����Լ�X������____���������Լ��ı�ţ���
A����������
B����ˮ
C����ʽ̼��ͭ
D������ͭ
(4)������н���ҺpH���ڵ��ķ�Χ��____��
(5)�����Ҫ�õ���ˮ�Ȼ�ͭ����Ҫ�ڸ����HCl�����м���CuCl2��xH2O����ԭ����____ ��
(6)����⣬CuCl2��xH2O�к�ˮ28. 6%����CuCl2��xH2O��x��ֵΪ____��
(7)���������80%���Ȼ�ͭת�뾧�壬�������ת��������ȫ�ģ����������ͼ�б�ʾ���������ݣ�д�� ��Ʒ������ͭ���������ļ���ʽ��
�ο��𰸣�(1)����������ֽ
(2)CuO+2H+==Cu2++H2O��FeO+ 2H+=Fe2++H2O
(3)B
(4)3. 7��5.2
(5)����HCl���� ���ȿ�����Cu2+��ˮ�⣬���ܴ���CuCl2��xH2O���Ȳ�����ˮ ��
(6)3
(7)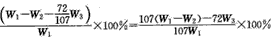
���������
�����Ѷȣ�һ��
3������� �����ǹ�ҵ�������ճ������е���Ҫ���ʣ�ij��ȤС��Ϊ�ⶨij��ҵ����������̼���������ʣ���̼���Ƶ������������������������ʵ�鷽������̽��������գ�
����һ��������Ʒ
�ⶨʣ���������
��1���ֱ��ȡ���������ʹ�����Ʒ����������������Ʒ���������г�ּ��ȣ�����ͼ���������з�����Ӧ�Ļ�ѧ����ʽΪ��______��
��2�����������ڸ���������ȴ�������ʵ��ʱ��Ҫ�ظ������ȡ���ȴ��������������Σ���Ŀ���ǣ�______��

��������������Ʒ��Һ�ⶨ��������
��1����ȡm1g��Ʒ������С�ձ��У���ˮ�ܽ⣮��С�ձ��еμ������Ȼ�����Һ����ͼ��������Ӧ�������˺����һ�������ǣ�______��
��2����������������Ϊm2g�������Ʒ��̼���Ƶ���������Ϊ��______��
��3�����������������Һ�����Ȼ�����Һ����������������������ȷ������£������Ʒ�е�̼����������������ʵ��______���ƫ�ߡ�����ƫ�͡����䡱����
��������������Ʒ�ⶨ���ɶ�����̼������
��1����ʵ�����vkͼװ�ã�C��ʢ�ŵ�������______��
��2����Ӧǰ��Ҫͨ��N2����Ӧ��ͨ��N2��Ŀ���ǣ�______

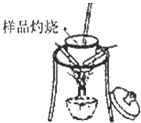
�ο��𰸣�����һ��
��1�������з�����Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3=Na2CO3+CO2��+H2O
�ʴ�Ϊ��2NaHCO3=Na2CO3+CO2��+H2O����֤NaHCO3ȫ���ֽ⣮
��2���÷������ݼ��Ⱥ��������������⣬Ҫ���������أ��Ա�֤NaHCO3ȫ���ֽ⣮
�ʴ�Ϊ�����������أ��Ա�֤NaHCO3ȫ���ֽ⣮
��������
��1��̼��Ƴ����ḽ���Ȼ��ơ��Ȼ��ƣ����˺���������ˮϴ�ӣ�
�ʴ�Ϊ��������ˮϴ�ӣ�
��2����������������Ϊm2g��̼������ʵ�������̼�������ʵ���������̼���Ƶ�����Ϊm2100��106g�������Ʒ��̼���Ƶ���������Ϊm2100��106gm1g��100%=106m2m1%��
�ʴ�Ϊ��106m2m1%��
��3����һ������Ʒ�м�������Ca��OH��2��Һ����ʱ�ֱ������·�ӦNa2CO3+Ca��OH��2=CaCO3��+2NaOH��
NaHCO3+Ca��OH��2=CaCO3��+NaOH+H2O��������CaCO3������������Ʒ������������CaCO3�������������Լ���̼�����������Ϳɵó������������������������������Һ�����Ȼ�����Һ����������������������ȷ������£������Ʒ�е�̼���������������䣮
�ʴ�Ϊ�����䣮
��������
��1��Cװ�ø��������̼������C��ʢ�ŵ�������Ũ���ᣮ
��2���÷����ؼ���Ҫ��ò�����CO2��������ʵ��ǰ�����ں��п����������к��ж�����̼����Ӱ�����ɵĶ�����̼��������Ӧ��װ���������ں��ж�����̼�����ܱ�C�м�ʯ����ȫ���գ����²ⶨ����нϴ������Է�Ӧǰ��Ҫͨ��
N2����Ӧ��ͨ��N2��Ŀ���ǣ��ž�װ���ڵĿ����������ɵĶ�����̼���������ų�����Dװ���м�ʯ�����գ�
�ʴ�Ϊ���ž�װ���ڵĿ����������ɵĶ�����̼���������ų�����Dװ���м�ʯ�����գ�
���������
�����Ѷȣ�һ��
4������� һ��ѧ�о���ѧϰС���ij��������ӡˢ��·������÷�Һ����̽��������ԭ����2Fe3++Cu�T2Fe2++Cu2+�����밴Ҫ���������̽�����森
[̽��Ŀ��]
�ӷ�Һ�л���ͭ�������µõ�FeCl3��Һ��
[���ϻ�Ϥ]
��3Fe2++NO3-+4H+�T3Fe3++NO��+2H2O
���йؽ������Ӵӿ�ʼ������������ȫʱ��Һ��pH��
Fe3+��2.7��3.7Cu2+��5.2��6.4Fe2+��7.6��9.6
[̽��˼·]
��1����ȷ����Һ����ɼ����������ӵ�Ũ�ȣ�
��2��ѡ������Լ�����ͭ�������µõ�FeCl3��Һ��
[ʵ��̽��]
ȡ���η�Һ���Թ��м�ˮϡ�ͺμ�KSCN��Һ����Ѫ��ɫ����֪��Һ�г�����Fe2+��Cu2+�⣬������Fe3+��
��ͬѧȡ10mL��Һ�������м���������AgNO3��Һ���õ��ij��������ˡ�ϴ�ӡ��������8.61g����ͬѧ��ȡ10mL��Һ������ij�Լ���pH����4.0��ʹ����Fe3+ת��ΪFe��OH��3��������Fe2+��Cu2+�����ڷ�Һ�У����������ˡ�ϴ�ӡ����գ���ȴ����ص�0.32g��
ͨ�������֪��Һ��c��Fe3+��=______mol/L��c��Fe2+��=______mol/L��c��Cu2+��=______mol/L��
[��������]
��λ���1L��Һ�к��е�ͭ�������µõ�FeC13��Һ��
��ͬѧ��ΪӦ�������Һ�м���wg����[w=c��Cu2+����1L��56g/mol]��ʹ֮��ַ�Ӧ�û���ͭ�����ˣ��ý���ͭ��������Һ�м���������ϡ���ᣬ��Fe2+ȫ������ΪFe3+��������β�����������ɴ�ʵ��Ŀ�ģ���Щͬѧ��Ϊ��ͬѧ�ķ��������У��������۱�ͬѧ�ķ�������Щ����֮��������һ��������
��1��______��2��______��3��______
��С��ͬѧ�������۵õ��ĺ����������в��������մﵽ��Ԥ��Ŀ�ģ������������ԣ�
[��չ����]
�뻭��1L��Һ�м������۵����ʵ������Һ��ͭ���ӵ����ʵ����Ĺ�ϵ���ߣ�������ͼ����㣬��ͭ���ӵ����ʵ�������һ��ʱ���������۵�������______g��

�ο��𰸣�[ʵ��̽��]��ͬѧʵ������ĵ���8.61g����Ϊ�Ȼ��������ʵ�����0.06mol����Cl-���ʵ���Ϊ0.06mol����ͬѧpH����4.0ʱ��ֻ��Fe3+�������ҳ�����ȫ������Ϊ�������������յõ�0.32gFe2O3�����ʵ���Ϊ0.002mol������Ԫ���غ��֪Fe3+�����ʵ���Ϊ0.004mol��c��Fe3+��=0.004mol0.01L=0.4 mol?L-1����2Fe3++Cu�TCu2++2Fe2+��֪2n��Cu2+��=n��Fe2+�����ɵ���غ��֪��3n��Fe3+��+2n��Cu2+��+2n��Fe2+��=n��Cl-������n��Cu2+��+n��Fe2+��=12��0.06mol-0.004mol��3��=0.024mol��n��Cu2+��+n��Fe2+��=n��Cu2+��+2n��Cu2+��=0.024mol����ã�n��Cu2+��=0.008mol��c��Cu2+��=0.008mol0.01L=0.8 mol?L-1����
n��Fe2+��=2n��Cu2+��=0.016mol��c��Fe2+��=0.016mol0.01L=1.6 mol?L-1��
�ʴ�Ϊ��0.4��1.6��0.8��
[��������]��������������֪��c��Fe3+��=0.4 mol?L-1��c��Cu2+��=0.8 mol?L-1������wg���ۣ������������㣬��Һ���в�����ͭ���ӣ�ʹ������������������Ӧ��������������������ӣ�
�ʴ�Ϊ���������۲��㣬��Һ���в�����Cu2+����HNO3�������������µ�����NO3-��
[��չ����]������1L��Һ����n��Fe3+��=0.4mol��n��Cu2+��=0����8mol�����ȷ���Fe+2Fe3+=3Fe2+ ����Cu2++Fe=Fe2++Cu��0.4molFe3+����0.2molFe����ʱn��Cu2+��=0.8mol���õ����꣨0.2��0.8����Ȼ��Cu2++Fe=Fe2++Cu��Ӧ�������������ʵ�����Cu2+���ٵ����ʵ�����ȣ��ɵõ����¼������꣨0.4��0.6������0.6��0.4����0.8��0.2������1.0��0�����������Ϲ�ϵ���Ի���1L��Һ�м������۵����ʵ������Һ��ͭ���ӵ����ʵ����Ĺ�ϵ���ߣ�
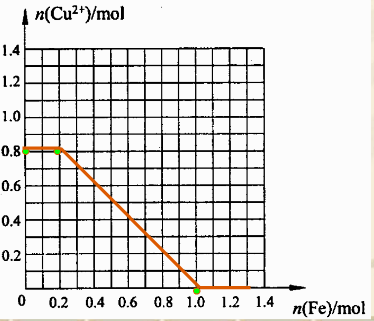 ��
��
��ͭ�������ʵ�����Ϊ0.4molʱ�������������ʵ���Ϊ0.6mol������Ϊ0.6mol��56g/mol=33.6g��
�ʴ�Ϊ�� ��33.6��
��33.6��
���������
�����Ѷȣ���
5������� ij��ѧС���ͬѧ��ʵ����ѧϰ����ͼ1��ʵ�����ϰ�������������
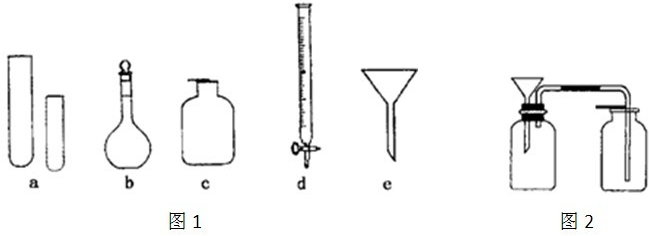
��1��ָ����ʦҪ��ͬѧ��д�����������ƣ���ͬѧ��д�Ĵ����±��������ҳ����еĴ����������������д���±��У�����ȷ����ÿղ���Ҫ��д����
| ������� | a | b | c | d | e
����
�Թ�
����ƿ
����ƿ
��ʽ�ζ���
��ͨ©��
����������
______
______
______
______
______
|
��2������e����;����ͬѧ˵����ɷ�����װ�ã��㻹��˵������������;��
��______��
��______��
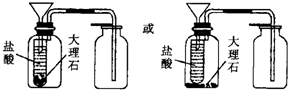
��3����ͬѧ����ͼ2װ���Դ���ʯ��ϡ���ᷴӦ��ȡCO2����ʦָ��������Ҫ̫���ϡ���ᣬ����˷ѣ���ͬѧѡ���������һ������������װ���ϣ������������⣮����Ѹ���������ͼ�к��ʵ�λ�ã�
�ο��𰸣���1��b�к���д����Ӧ��Ϊ����ƿ��d��������ʽ�ζ��ܣ���ʽ�ζ����л�������ʽ�ζ����¶����ܣ������в�����
�ʴ�Ϊ���������bd���Ƹ�������������ƿ��ʽ�ζ��ܣ�2��©�����¿ڽ�ϸ������������;�Т���ϸ�������м�Һ�壻����ɹ���װ�ã�
�ʴ�Ϊ������ϸ�������м�Һ�壻����ɹ���װ�ã�
��3��©����̫�̣������Ķ�����̼������©����й¶����©�����¼�һֻС�Թܣ��Թ��ڼ���ϡ�����©�����⣬������������������ʯ��Ӧ����ȡ������̼��
�ʴ�Ϊ��
���������
�����Ѷȣ�һ��