| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ�㽲�⡶ԭ���ԭ������Ƶ����Ԥ�⣨2017�����°棩(��)
(2)Ŀǰ��ҵ����һ�ַ�������C02�������״���Ϊ̽���䷴Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g)  CH3OH(g)+H2O(g)? ��H=-49.0kJ��m01-1�����C02��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ�� CH3OH(g)+H2O(g)? ��H=-49.0kJ��m01-1�����C02��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ�� �ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ���ʣ�v(H��)=??�� �ڸ÷�Ӧ��ƽ�ⳣ��Ϊ?�� (3)��KHC03��ҺΪ����ʣ��õ��ķ���Ҳ���Խ�CO2��ԭΪ�״�����д�����ʱ���������ӷ���ʽ��? (4)���ʯ��ʯīϩ������̼��̼�ļ���ͬ�������塣�Ӽ������ͷ������ǵ��ȶ�����ǿ������˳��Ϊ?  �ο��𰸣���10�֣� ���������(1)ȼ�յı�Ҫ�����ǿ�ȼ��ﵽ�Ż������������������̼���������Ҫ�Dz��ý���ȼ������������İ취�ﵽĿ�� �����Ѷȣ��� 2��ѡ���� ����������ԭ��������ԭ�����ɵ��ǣ������� �ο��𰸣�A�������ʵ�п�����γ�ԭ��أ�����п������ʱ�ȴ�п���ᷴӦ�죬������ԭ�����ɵģ���A���� ��������� �����Ѷȣ��� 3��ѡ���� ����ͼ�����жϳ��������ӷ���ʽ�д�����ǣ������� |

�ο��𰸣�A������ͼʾ��Ӧԭ����֪����Cd������ǿ��Ag������Cd�����û�Ag����A����
B������ԭ��صĹ�����������֪����ͼ��ʾװ����ԭ��صĹ���װ�ã�װ��1��CdΪ����������Cd�û�Co�ķ�Ӧ��˵��Cd�Ļ�����ǿ��Co����B��ȷ��
C������ͼʾ��Ӧԭ����֪����Cd������ǿ��Ag������Cd�����û�Ag����C��ȷ��
D��װ��2��CoΪ����������Co�û�Ag�ķ�Ӧ��˵��Co�Ļ�����ǿ��Ag������Co�û�Ag�ķ�Ӧ����D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
4������� �о������ḻ��CO2��ȫ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ(ʯ�ͺ���Ȼ��)����������Ҷ���ݽߵ�Σ����ͬʱ�ֿɻ�����CO2�ۻ�������������ЧӦ��ʵ��CO2������ѭ����
��1��Ŀǰ��ҵ����һ�ַ�������CO2��H2��230�����������ת�����ɼ״�������ˮ��������ͼ��ʾ��ѹ������0.5 mol CO2��1.5 mol H2ת���ʴ�80%ʱ�������仯ʾ��ͼ��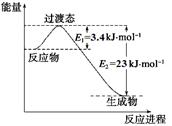
��д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� ��
a��������ѹǿ���� b��H2�������������
c��c(H2)=3c(CH3OH) d���������ܶȲ���
e��2��C��O���ѵ�ͬʱ��6��H��H���ѡ�
��2���˹���������ܹ�����̫���ܣ���CO2��H2O�Ʊ���ѧԭ�ϣ���ͼ��ͨ���˹���������Ʊ�HCOOHԭ����ʾ��ͼ������Ҫ��ش����⣺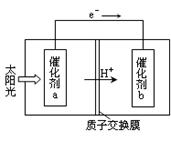
�ٸù����ǽ� ת��Ϊ ��(��������ѡ����ܡ���̫���ܡ�����ѧ�ܡ�)
�ڴ���b����ĵ缫��Ӧ����ʽΪ ��
��3��ij��������Ա�����ʹ�����������ͣ����ͻ�ѧʽ��C8H18��ʾ�����ȼ�ϵķ������Խ������CO2���ŷ����⡣�÷�����Ҫ���ô������CaH2����H2������������������������ʹ�ã�����ϵͳ�ֲ�������ȼ�ղ�����CO2����ϵͳ��Ӧ����ͼ��ʾ��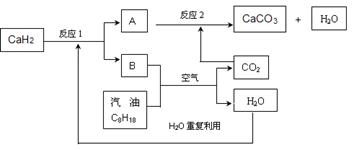
����������⣺
��д��CaH2�ĵ���ʽ ��
�ڷ�Ӧ1���������뻹ԭ�������ʵ���֮���ǣ� ��
�����ϵͳ��Ӧ��������ȫ����д����ϵͳ�ܷ�Ӧ�Ļ�ѧ����ʽ ��
�ο��𰸣�
��1����CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H =��49 kJ��mol-1(3��))��bd (2�֣���ѡ��ѡ0�֣�©ѡ1����1��)
CH3OH(g)+H2O(g) ��H =��49 kJ��mol-1(3��))��bd (2�֣���ѡ��ѡ0�֣�©ѡ1����1��)
��2����̫���� ��ѧ��(��1��) ��CO2+2e��+2H+=HCOOH(2��)
��3����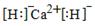 (2��)
(2��)
��2��1 (2��) ��16CaH2+ 2C8H18+41O2=16CaCO3+34 H2O(2��)
�����������1���������������仯ʾ��ͼ��֪��1mol CO2��3molH2ת���ʴ�100%ʱ�ų�����49kJ�����Ը÷�Ӧ���Ȼ�ѧ����ʽΪ��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H =��49 kJ��mol-1
CH3OH(g)+H2O(g) ��H =��49 kJ��mol-1
��a���÷�Ӧ���ں�ѹ�����н��У�����ѹǿʼ�ղ��䣬�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬������b����ƽ��ʱ�������ʵĺ��������ٸı䣬��������������㶨�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����ȷc��ƽ��ʱ�������ͼ״���Ũ�Ȳ�һ���߱���ѧ�������ı�����ϵ�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬������d�����ڸ÷�Ӧ�Ƿ�Ӧǰ����������ʵ����ı�ķ�Ӧ����ѹǿ����ʱ����������ڼ�С���ܶ�����ƽ��ʱ�����ܶȲ��������ֲ��䣬���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����ȷ��e����Ӧ���κ�״̬ʱ����2��C��O���ѵ�ͬʱ��6��H��H���ѣ������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬������ѡbd��
��2���ٸ�ͼ������̫���ܽ�������̼ת��ΪHCOOH�������ǰ�̫����ת��Ϊ��ѧ�ܣ��ڸ��ݵ��ӵ�����������b�൱��ԭ��ص�������������ԭ��Ӧ�����Է����ķ�ӦΪCO2+2e��+2H+=HCOOH��
��3����CaH2�����ӻ���������ʽΪ ��
��
�ڷ�Ӧ1��CaH2��H2O��Ӧ�����������ƺ���������Ӧ��CaH2����ԭ����ˮ������������д�������Ļ�ѧ����ʽCaH2+2H2O=Ca(OH)2+H2���������������뻹ԭ�������ʵ���֮����2:1��
���ɷ�Ӧ������ͼ��֪�����ղ�����CaCO3��H2O����Ӧ1���ɵ�������������Ӧ����ˮ��������������Ӧ���ɶ�����̼��ˮ�����ж�����̼���ںͷ�Ӧ1�������������Ƶķ�Ӧ����������Ӧ�Ļ�ѧ����ʽ���ӣ���ȥ�м���������̼���������������ƣ����IJ���ֻ��ˮ��̼��ƣ������ܷ�Ӧ����ʽΪ16CaH2+ 2C8H18+41O2=16CaCO3+34H2O��
���㣺�����Ȼ�ѧ����ʽ������ʽ���缫��Ӧʽ����д����ѧƽ����жϣ�����ת�����жϣ�����ʽ���ӷ���Ӧ��
�����Ѷȣ�����
5������� X��Y��Z���ǽ�������XͶ��Z����������Һ��,X�ı�����Z������X ��Y���ԭ���ʱ��YΪ��صĸ�����X��Y��Z���ֽ����Ļ�����˳��Ϊ?.
�ο��𰸣�Y>X>Z
���������X�ܰ�Z������������Һ���û�������˵��X�Ļ�����ǿ��Z��X ��Y���ԭ���ʱ��YΪ��صĸ�����˵��Y�Ļ�����ǿ��X������ȷ��ΪY>X>Z
�����Ѷȣ���
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ�����л�ѧ֪ʶ���ȫ����Ӧ������.. | ||
| �����Ŀ |