微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知H2(g) + Cl2(g) == 2HCl(g);△H=
2、填空题 黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.100?0g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.020?0?mol/L的K2Cr2O7
标准溶液滴定至终点,消耗,K2Cr2O7溶液25.00?mL。 ?
已知:SO2+2Fe3+?+2H2O=SO42-?+2Fe2+?+4H+ ?Cr2O2-?+6Fe2+?+14H+=2Cr3+?+6Fe3+?+7H2O?
(1)样品中FeS2的质量分数是(假设杂质不参加反应)____________________。 ?
(2)若灼烧69?FeS2产生的SO2全部转化为SO3气体时放出9.8?3kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式:
________________________。 ?
(3)煅烧10?t上述黄铁矿,理论上产生SO2的体积(标准状况)为_______L,制得98%的硫酸质量为_______t,SO2全部转化为H2SO4时放出的热量是________kJ。
3、选择题 化学反应N2+3H2=2NH3的能量变化如下图所示,该反应的热化学方程式是

[? ]
A.N2(g)+3H2(g) === 2NH3(1) △H=2(a-b-c)kJ・mol-1
B.N2(g)+3H2(g) === 2NH3(g) △H=2(b-a)kJ・mol-1
C.N2(g)+H2(g) === NH3(1) △H=(b+c-a)kJ・mol-1
D.N2(g)+H2(g) === NH3(g) △H=(a+b)kJ・mol-1
4、选择题 已知下列热化学方程式
(l)C(s)+1/2O2(g)=CO(g) △H1=-110.5kJ/mol
(2)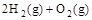 =2H2O(g) △H2=-483.6 kJ・
=2H2O(g) △H2=-483.6 kJ・
由此可知 C(s)+ H2O(g) == CO(g) + H2(g) △H3。则 ΔH3等于( )
A.+131.3kJ・mol―1
B.-131.3kJ・mol―1
C.+373.1kJ・mol―1
D.-373.1kJ・mol―1