| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《热化学方程式》考点巩固(2017年最新版)(六)
参考答案:C 本题解析:醋酸是弱酸,存在电离平衡,电离是吸热的,所以醋酸和氢氧化钠溶液反应放出的热量少。浓硫酸溶于水放出大量的热,所以正确的答案选C。 本题难度:一般 2、填空题 (12分)近年来我国汽车拥有量呈较快增长趋势,NOx是汽车尾气中的主要污染物之一。 |
 2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率 (填“增大”、“减小”或不变,下同),N2的体积分数 。
2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率 (填“增大”、“减小”或不变,下同),N2的体积分数 。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4mol・L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)(×10-3 mol・L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
参考答案:(1) ① N2(g)+O2(g)=2NO(g) △H="+183" kJ/mol (2分) > (1分) ②A、C(2分)
(2)减小(1分) 增大(2分)
(3)①2NO+2CO N2+2CO2(2分) ②1.88×10-4 mol/(L・s) (2分)
N2+2CO2(2分) ②1.88×10-4 mol/(L・s) (2分)
本题解析:(1)①由题可知,该反应的热化学方程式为:N2(g)+O2(g)=2NO(g) △H=(945+498-2×630)kJ/mol="+183" kJ/mol;该反应在高温下为自发进行故△G=△H-T△S<0,可知该反应△S>0;②根据右图所示,只改变条件R,当N2的转化率从a3到a1时,平衡正向移动,可采取措施:升高温度平衡常数K增大,或增大氧气量,平衡常数不变,故应选AC;(2) 氮气是合成氨的原料之一,合成氨反应:N2(g)+3H2 (g) 2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,反应逆向进行达到新的平衡时,H2的转化率减小;N2的体积分数增大;(3)在汽车上安装高效催化转化器,将有毒气体转化为无毒气体,可有效降低NOx的排放,①写出反应的化学方程式:2NO+2CO
2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,反应逆向进行达到新的平衡时,H2的转化率减小;N2的体积分数增大;(3)在汽车上安装高效催化转化器,将有毒气体转化为无毒气体,可有效降低NOx的排放,①写出反应的化学方程式:2NO+2CO N2+2CO2;②前2 s内的平均反应速率ν(NO) =
N2+2CO2;②前2 s内的平均反应速率ν(NO) = mol/(L・s),则ν(N2)=1/2ν(NO)=1.88×10-4 mol/(L・s)。
mol/(L・s),则ν(N2)=1/2ν(NO)=1.88×10-4 mol/(L・s)。
考点:化学反应原理综合。
本题难度:困难
3、填空题 (1)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ・mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=-47.4kJ・mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5kJ・mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
。
(2)在压强为0.1 MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g);CO的转化率与温度、压强的关系如图所示。
CH3OH(g);CO的转化率与温度、压强的关系如图所示。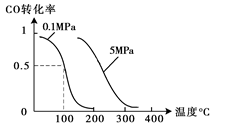
①该反应的△H 0 (填“<”、“>”或“=”)。
②在温度容积不变的情况下,向该密闭容器再
增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”)。
(3)实验室中配制AgNO3溶液时通常需要向其中加入 ,目的是 ; AgCl在水中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)。25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号)。
Ag+(aq)+Cl-(aq)。25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号)。
参考答案:(1)CO(g)+FeO(s)===Fe(s)+CO2(g) △H=-218.0kJ/mol
(2)① <; ② 增大(3)硝酸 抑制Ag+水解
②①④③
本题解析:(1)CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式为CO(g)+FeO(s)===Fe(s)+CO2(g) △H的计算如下,将3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)加上Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) 乘以2,得到3Fe2O3(s)+ 3CO(g)=6FeO(s)+3CO2(g),化简得到Fe2O3(s)+ CO(g)=2eO(s)+CO2(g),
△H=1/3(-47.4kJ・mol-1+2×+640.5)=411.2kJ・mol-1,将Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)减去Fe2O3(s)+ CO(g)=2FeO(s)+CO2(g),化简得到2FeO(s)+2 CO(g)=2Fe(s)+2CO2(g) ,
△H=-24.8-411.2=-436kJ/mol,所以CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式为CO(g)+FeO(s)===Fe(s)+CO2(g) △H=-218.0kJ/mol;
(2)①由图可以知道,温度升高,CO的转化率减小,所以该反应为放热反应,故△H<0,②在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,相当于增大压强,反应向正方向移动,所以CO的转化率增大;
(3)由于银离子易水解,所以配制AgNO3溶液时通常需要向其中加入硝酸,目的是抑制Ag+水解,AgCl(s) Ag+(aq)+Cl-(aq),在①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液中,充分搅拌后,相同温度下Ag+浓度由大到小的顺序是②①④③。
Ag+(aq)+Cl-(aq),在①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液中,充分搅拌后,相同温度下Ag+浓度由大到小的顺序是②①④③。
考点:热化学方程式的书写,化学平衡
点评:本题考查了热化学方程式的书写,化学平衡,第一小题的计算比较繁杂,后面两个小题比较容易。
本题难度:困难
4、简答题 (1)H2S的燃烧热△H=-akJ?mol-1,则H2S燃烧反应的热化学方程式为______.
(2)已知:高温下,在密闭容器中用H2还原WO2可得到金属钨.当温度过高时,WO2(s)会转变为WO2(g).请根据以下反应:
WO2(s)+2H2(g)?W(s)+2H2O(g);△H=+66.0kJ?mol-1
WO2(g)+2H2?W(s)+2H2O(g);△H=-137.9kJ?mol-1
计算出WO2(s)?WO2(g)的△H=______.
(3)工业上常利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,反应的化学方程式为:
CH4+CO2=2CO+2H2
已知CH4、H2和CO的燃烧热分别为890.3kJ?mol-1、285.8kJ?mol-1、283.0kJ?mol-1,则生成1m3(标准状况)CO所需热量为______.
参考答案:(1)H2S的燃烧热△H=-a kJ?mol-1,由燃烧热概念可知2mol硫化氢燃烧放热2aKJ,则H2S燃烧反应的热化学方程式为2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-2akJ?mol-1,
故答案为:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-2akJ?mol-1;
(2)①WO2 (s)+2H2 (g)?W (s)+2H2O (g)△H=+66.0kJ?mol-1
②WO2 (g)+2H2?W (s)+2H2O (g)△H=-137.9kJ?mol-1
由盖斯定律①-②计算出WO2 (s)?WO2 (g) 的△H=+203.9 kJ?mol-1,
故答案为:+203.9kJ?mol-1;
(3)已知CH4、H2和CO的燃烧热分别为890.3kJ?mol-1、285.8kJ?mol-1、283.0kJ?mol-1,热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1
②H2(g)+12O2(g)=H2O(l)△H=-285.8kJ?mol-1
③CO(g)+12O2(g)=CO2(g)△H=-283.0kJ?mol-1
依据盖斯定律①-②×2-③×2得到:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247KJ/mol,
则生成1m3(标准状况)CO物质的量=1000L22.4L/mol,所需热量=100022.4mol×247KJ2mol=5.52×103kJ,
故答案为:5.52×103kJ.
本题解析:
本题难度:一般
5、选择题 化学反应N2+3H2=2NH3的能量变化如下图所示,该反应的热化学方程式是
[? ]
A.N2(g)+3H2(g) === 2NH3(1) △H=2(a-b-c)kJ・mol-1
B.N2(g)+3H2(g) === 2NH3(g) △H=2(b-a)kJ・mol-1
C.N2(g)+H2(g) === NH3(1) △H=(b+c-a)kJ・mol-1
D.N2(g)+H2(g) === NH3(g) △H=(a+b)kJ・mol-1
参考答案:A
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:下列实验操作不正确的是( )A.. | |