微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下, 浓度均为0. 1 mol/L的6种溶液的pH如下表:
序号
| a
| b
| c
| d
| e
| f
|
溶质
| CH3COONa
| NaHCO3
| Na2CO3
| NaClO
| NaCN
| NaAlO2
|
pH
| 8. 8
| 9. 7
| 11. 6
| 10. 3
| 11. 1
| 11. 3
|
(1)上述溶液中的阴离子结合H+能力最弱的为 。(填阴离子化学式)
(2)NaAlO2溶液呈碱性的原因是 (用离子方程式表示)。将溶液加热蒸干最后得到的固体产物是 ;
(3)结合表中数据分析, 与0. 1 mol/L的CH3COONa溶液中水的电离程度相同的有 (填字母代号)。
A.pH="8." 8的NaOH溶液 B. pH="5." 2的NH4Cl溶液 C.pH="5." 2的盐酸
D. 0. 1 mol/L的NaCN溶液 E.pH="8." 8的Na2CO3溶液
(4)将浓度均为0. 1 mol/L的b、c等体积混合, 所得溶液中各离子浓度关系正确的有 。
A.c(Na+)= c(CO32-) +c(HCO3-) +c(H2CO3)
B. 2c(Na+)=3c(CO32-) +3c(HCO3-) +3c(H2CO3)
C. c(OH-)= c(H+) +c(HCO3-) +2c(H2CO3)
D. c(Na+) +c(H+) = 2c(CO32-) +c(HCO3-) +c(OH-)
E. c(Na+)>c(HCO3-)> c(CO32-) > c(OH-)> c(H+)
F. c(Na+)> c(CO32-) > c(HCO3-) > c(H+)> c(OH-)
(5)0.2 mol/LHCl与0.1 mol/L NaAlO2溶液等体积混合溶液后离子浓度顺序为 。
参考答案:(1)CH3COO- (2)AlO- +2H2O  Al(OH)3+OH- , NaAlO2
Al(OH)3+OH- , NaAlO2
(3) BE (4)BDE (5)c(Cl- )>c(Na+)>c(Al3+)>c(H+)>c(OH- )
本题解析:
(1)相同浓度的钠盐溶液,pH越小则盐的水解程度越小,阴离子结合H+能力最弱的就是弱酸根对应的酸酸性最强的。酸性强弱CH3COOH>H2CO3>HClO>HCN>HAlO2,所以阴离子结合H+能力最弱的为CH3COO-。
(2)NaAlO2是强碱弱酸盐,AlO-水解使溶液显碱性,AlO- +2H2O Al(OH)3+OH- , NaAlO2水解生成NaOH和Al(OH)3,二者均不易分解和挥发,所以将溶液加热蒸干最后得到的固体产物是NaAlO2。
Al(OH)3+OH- , NaAlO2水解生成NaOH和Al(OH)3,二者均不易分解和挥发,所以将溶液加热蒸干最后得到的固体产物是NaAlO2。
(3)0.1mol/L的CH3OONa溶液,促进水的电离,水电离的c(OH-)=10?14 /10?8.8 =10-5.2mol/L
A.pH=8.8的NaOH溶液,抑制水的电离,水电离的c(H+)=10-8.8mol/L;
B.pH=5.2的NH4Cl溶液,促进水的电离,水电离的c(H+)=10-5.2mol/L;
C.pH=5.2的盐酸,抑制水的电离,水电离的c(OH-)=10?14 /10?5.2 =10-8.8mol/L;
D.0.1mol/L的NaCN溶液,促进水的电离,水电离的c(H+)=10-11.1mol/L;
E.pH=8.8的Na2CO3溶液,促进水的电离,水电离的c(OH-)=10?14 /10?8.8 =10-5.2mol/L;
所以与0.1mol/L的CH3OONa溶液中水的电离程度相同的是:BE;故答案为:BE;
(4)将浓度均为0. 1 mol/L的NaHCO3、Na2CO3等体积混合,混合溶液中粒子之间符合电荷守恒,物料守恒和质子守恒。NaHCO3溶液有物料守恒:c(Na+)=c(CO32-) +c(HCO3-) +c(H2CO3);Na2CO3溶液有c(Na+)=2c(CO32-) +2c(HCO3-) +2c(H2CO3;二式相加即2c(Na+)=3c(CO32-) +3c(HCO3-) +3c(H2CO3;B正确。电荷守恒c(Na+) +c(H+) = 2c(CO32-) +c(HCO3-) +c(OH-)D正确; CO32-水解程度大于HCO3-,溶液呈碱性,所以有c(Na+)>c(HCO3-)> c(CO32-) > c(OH-)> c(H+) ,E正确。
考点:本题考查盐类水解素、化学平衡的影响因素、
本题难度:困难
2、填空题 化合物SOCl2是一种液态化合物,沸点为77℃。在盛10ml水的锥形瓶中小心滴加8-10滴SOCl2可观察到剧烈反应,液面上形成白雾,并有刺激性气味的气体放出,该气体可使湿润的品红试纸褪色。在反应后的溶液中滴加AgNO3溶液,可生成一种不溶于稀HNO3的白色沉淀。
(1)试据上述实验事实,写出SOCl2与水反应的化学方程式 。
(2)将ZnCl2溶液蒸发至干,得不到无水ZnCl2,工业上常用ZnCl2?2H2O与SOCl2共热制取ZnCl2。试结合离子方程式解释原因: 。
(3)科学家经常利用 水解原理制备纳米材料,请写出用TiCl4制备TiO2・xH2O的化学方程式: 。
水解原理制备纳米材料,请写出用TiCl4制备TiO2・xH2O的化学方程式: 。
参考答案:
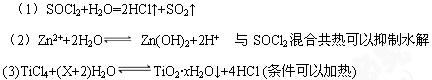
本题解析:略
本题难度:困难
3、填空题 (12分)
(1)实验室在临时配制一些FeCl2的溶液时,常将氯化亚铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,是为了 。稀释后还需要加入一些铁粉,其目的是 ,相关反应的离子方程式为 。
(2)氯化铁水溶液呈 性 ,原因是(用离子方程式表示):
_____________________ ____ 。把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。如果要从氯化铁溶液得到纯氯化铁固体,常采用的方法是 。
参考答案:(12分)(1)抑(防)止Fe2+水解(2分); 防止Fe2+被氧化成Fe3+(2分) ;
2Fe3+ + Fe = 3Fe2+ (2分)
(2)酸性(1分); Fe3+ + 3H2O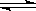 Fe(OH)3 + 3H+(2分,写“=”不得分)
Fe(OH)3 + 3H+(2分,写“=”不得分)
氧化铁或Fe2O3(1分); 将三氯化铁溶液在HCl环境(或气氛)中加热蒸干(2分)
本题解析:略
本题难度:一般
4、填空题 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
元素
| 有 关 信 息
|
A
| 元素主要化合价为-2,原子半径为0.074 nm
|
B
| 所在主族序数与所在周期序数之差为4
|
C
| 原子半径为0.102 nm,其单质为黄色晶体,可在A的单质中燃烧
|
D
| 最高价氧化物的水化物能按1
|
参考答案:
本题解析:
本题难度:困难
5、选择题 下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
①在0.1 mol・L-1 NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
②在0.1 mol・L-1 Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
③向0.2mol・L-1NaHCO3溶液中加入等体积0.1mol・L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
④常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol・L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
A.①④
B.②④
C.①③
D.②③