| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《铁的氧化物》高频试题巩固(2017年最新版)(五)
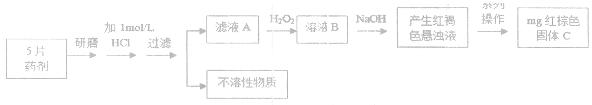 请回答下列问题: ①该小组发现将片状补血剂长  时间置于空气中,表面“发黄”,请用化学方程式表示原因?。 时间置于空气中,表面“发黄”,请用化学方程式表示原因?。②课外研究性小组发现在滤液A中滴入少量KClO溶液,并加入适量硫酸,溶液立即变黄。 甲同学推测该反应的还原产物有两种可能:①Cl2、②Cl- 乙同学结合甲的推测,认为其中一种可能可以排除,你认为可以排除的是(填序号)?;用离子方程式说明理由?。 ③若该实验温度下,上述红褐色难溶物质的溶度积为 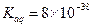 试计算该物质沉淀完全所需要的pH=?(要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3) 试计算该物质沉淀完全所需要的pH=?(要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)④若实验过程中无损耗,最后称量得到mg红棕色的固体,则每片补血剂中含铁元素的质量为?g(用含m的式子表示) ⑤丙同学认为蒸干灼烧溶液B,也可以制得红棕色固体C,请结合化学方程式加以说明 ?。 4、填空题 (8分)请回答下列各问: |
5、选择题 有一块铁的“氧化物”样品,用140mL 5.0mol・L-1 盐酸恰好将之完全溶解,所得溶液还能吸收0.025mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为
A.Fe2O3
B.Fe3O4
C.Fe4O5
D.Fe5O7
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《离子共存》.. | |