微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 燃料电池能量利用率可高达80%,下列说法错误的是
A.燃料电池的负极反应物是氢气、甲烷、乙醇等物质
B.氢氧燃料电池常用于航天飞行器,产物水经过处理之后可供宇航员使用
C.H2SO4作电解质,氢氧燃料电池的负极反应式H2+2OH--2e-=2H2O
D.乙醇燃料电池电解质为KOH,负极反应式C2H5OH+16OH--12e-=2CO32-+11H2O
参考答案:C
本题解析:A、原电池中负极失去电子发生氧化反应,氢气、甲烷以及乙醇等均是可燃物,所以燃料电池的负极反应物是氢气、甲烷、乙醇等物质,A正确;B、燃料电池的能量利用率高,产物无污染,所以氢氧燃料电池常用于航天飞行器,产物水经过处理之后可供宇航员使用,B正确;C、H2SO4作电解质,氢氧燃料电池的负极反应式H2-2e-=2H+,C不正确;D、乙醇燃料电池电解质为KOH,溶液显碱性,乙醇负极反应式C2H5OH+16OH--12e-=2CO32-+11H2O,D正确,答案选C。
本题难度:一般
2、简答题 某化学活动小组利用如下装置对原电池进行研究,请回答下列问题(其中盐桥为含有KCl溶液的琼脂).
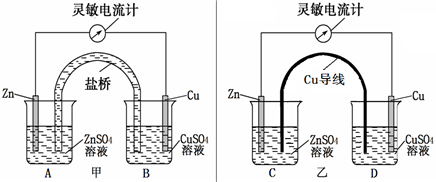
(1)、在甲图装置中,当电流计指针发生偏转时,盐桥中的离子移动方向为:K+移向______烧杯,Cl-移向______烧杯(填A或B),装置中电子转移的方向为:______.
(2)、如果将盐桥换成Cu导线(如乙图),该小组同学发现电流表指针仍然发生偏转,则C中可以构成______池,D中可以构成______池.
(3)、对乙图产生电流的原因猜想如下:
猜想一:ZnSO4溶液水解显酸性,如该观点正确,则C中铜导线上的电极反应式为:______.
猜想二:ZnSO4溶液酸性很弱,由于溶解了空气中的氧气而产生电流,如该观点正确,此时C中铜导线上的电极反应式为:______.
若猜想二正确,则可利用此原理设计电池为在偏远的海岛工作的灯塔供电,其装置以金属铝和石墨为电极,以海水为电解质溶液,试写出该电池工作时总反应的化学方程式______.
参考答案:(1)在甲图装置中,当电流计指针发生偏转时,形成原电池,锌为活泼金属,被氧化而失去电子,铜为原电池正极,正极上得电子而被还原,原电池中,电子由负极经外电路流向正极,电解质溶液中,阳离子向正极移动,阴离子向负极移动,
故答案为:B;A;由负极(Zn)沿导线移向正极(Cu);
(2)如果将盐桥换成Cu导线(如乙图),该小组同学发现电流表指针仍然发生偏转,则C中可以构成原电池,锌为活泼金属,被氧化而失去电子,铜为原电池正极,正极上得电子而被还原,分别连接电源的正负极,正极反应为Cu2++2e-=Cu,负极反应为Cu-2e-=Cu2+,为电解或电镀装置,
故答案为:原电;电解/电镀;
(3)ZnSO4溶液水解显酸性,Cu为正极,发生还原反应,电极反应为2H++2e-=H2↑,
ZnSO4溶液酸性很弱,由于溶解了空气中的氧气而产生电流,则正极发生还原反应,氧气在正极上得电子而被还原,电极反应为O2+4e-+2H2O=4OH-,
以金属铝和石墨为电极,以海水为电解质溶液,Al为负极,氧化反应,电极反应为Al-3e-+3OH-=Al(OH)3,正极反应为?O2+4e-+2H2O=4OH-,该电池工作时总反应的化学方程式为4Al+3O2+6H2O=4Al(OH)3,
故答案为:2H++2e-=H2↑;?O2+4e-+2H2O=4OH-;4Al+3O2+6H2O=4Al(OH)3.
本题解析:
本题难度:一般
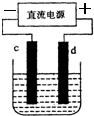
3、选择题 如图是电解氯化铜溶液的装置,c、d为石墨电极.则下列有关的判断正确的是( )
A.c是阴极,发生氧化反应
B.c是阳极,有H2放出
C.d是阳极,有Cl2放出
D.d是阴极,有Cu覆盖