| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《化学平衡状态的判断》在线测试(2017年最新版)(二)
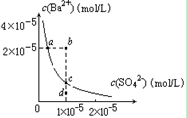 参考答案:B 本题解析:MgCl2在加热过程中会发生水解得不到MgCl2。电离常数表示其电离程度得相对大小。根据表中数据可知酸性强弱大小顺序为H2CO3[>HclO>HCO3-,因为酸越强,相应得盐越容易水解,即等物质的量浓度的NaClO、NaHCO3混合溶液中,前者的水解程度大于后者,且水解都显碱性,B正确。pH=2的稀硫酸,则稀硫酸的浓度为0.005mol/L,但在稀释过程中氢离子的物质的量是增加的,即氢离子的物质的量浓度略大于原来的十分之一,所以C不正确。D中a点是饱和溶液,当加入Na2SO4时增大c(SO42-),有晶体析出,所以c(Ba2+)减小。D点是不饱和溶液,若通过蒸发溶剂,变成饱和溶液,则c(SO42-)和c(Ba2+)均应该增大,D不正确。答案B。 本题难度:一般 3、选择题 一定温度下,在一定容的密闭容器中充入NO2发生如下反应:2NO2 参考答案:A 本题解析:】将继续充入的NO2在另一个容器中建立与原平衡相等条件的等效平衡后,再将其和原平衡压缩在一起建立平衡。由此可见,充入NO2相当于增大原平衡的压强,NO2的转化率增大。 本题难度:一般 4、选择题 可逆反应2NO2(g)?2NO(g)+O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是( ) 参考答案:①根据单位时间内生成n molO2的同时生成2n mol NO2 ,可知生成氧气的速率和消耗速率相等,达到了平衡状态,故①正确; 本题解析: 本题难度:简单 5、选择题 在密闭容器中将CO和水蒸气的混合物加热到800℃时,有下列平衡: 参考答案:D 本题解析:设参加反应的CO为xmol, 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《化学基本概.. | |