��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ʵ��������������ԭ����ƽ���ƶ�ԭ�������͵��ǣ�?��
���Ȼ�����Һ�����������յò����Ȼ������壻
�����ڳ�ʪ�Ŀ������������⣻
��ʵ���ҿ����ű���ʳ��ˮ�ķ����ռ�������
�ܱ���FeCl2��Һʱ����Һ�м�����������
�������Ȼ��ع����Ʊ���Na��L��+KCl��L��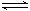 K��g��+NaCl��L����
K��g��+NaCl��L����
����������������������ƽ����ϵ����ѹ��С�������ɫ����
A���٢ڢ�
B���ڢܢ�
C���ۢܢ�
D���ڢݢ�
2������� 
 ij�¶�ʱ����2L�ܱ���������̬����X��Y��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯�����ʾ��
ij�¶�ʱ����2L�ܱ���������̬����X��Y��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯�����ʾ��
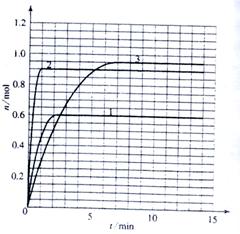

 ��1��������������ݣ�����ͼ�л���X��Y��Z�����ʵ�����n����ʱ�䣨t���仯�����ߣ�
��1��������������ݣ�����ͼ�л���X��Y��Z�����ʵ�����n����ʱ�䣨t���仯�����ߣ�
t/min
| X/mol
| Y/mol
| Z/mol
|
0
| 1.00
| 1.00
| 0.00
|
1
| 0.90
| 0.80
| 0.20
|
3
| 0.75
| 0.50
| 0.50
|
5
| 0.65
| 0.30
| 0.70
|
9
| 0.55
| 0.10
| 0.90
|
10
| 0.55
| 0.10
| 0.90
|
14
| 0.55
| 0.10
| 0.90
|

 (2) ��ϵ�з�����Ӧ�Ļ�ѧ����ʽ��___________________________;
(2) ��ϵ�з�����Ӧ�Ļ�ѧ����ʽ��___________________________;

 (3) ��ʽ����÷�Ӧ��0-3minʱ���ڲ���Z��ƽ����Ӧ���ʣ�_______________;
(3) ��ʽ����÷�Ӧ��0-3minʱ���ڲ���Z��ƽ����Ӧ���ʣ�_______________;

 (4) �÷�Ӧ�ﵽƽ��ʱ��Ӧ��X��ת����
(4) �÷�Ӧ�ﵽƽ��ʱ��Ӧ��X��ת����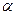 ����___________________________;
����___________________________;

 (5) ����÷�Ӧ�Ƿ��ȷ�Ӧ���ı�ʵ���������¶ȡ�ѹǿ���������õ�Z��ʱ��仯�����ߢ١��ڡ��ۣ�����ͼ��ʾ�������ߢ١��ڡ�������Ӧ��ʵ�������ı�ֱ��ǣ�
(5) ����÷�Ӧ�Ƿ��ȷ�Ӧ���ı�ʵ���������¶ȡ�ѹǿ���������õ�Z��ʱ��仯�����ߢ١��ڡ��ۣ�����ͼ��ʾ�������ߢ١��ڡ�������Ӧ��ʵ�������ı�ֱ��ǣ�

 �� _________________?��________________?��__________________
�� _________________?��________________?��__________________



3��ѡ���� һ�������¿��淴Ӧ��2A��g�� B��g��+3C��g������������״̬ʱ����ƽ��״̬���ǣ�������
B��g��+3C��g������������״̬ʱ����ƽ��״̬���ǣ�������
����Ӧ�����淴Ӧ���ʣ�
A������Ӧ���ʣ�v��A��=2mol?L-1?s-1
�淴Ӧ���ʣ�v��C��=2mol?L-1?s-1
B������Ӧ���ʣ�v��A��=2mol?L-1?s-1
�淴Ӧ���ʣ�v��B��=1.5mol?L-1?s-1
C������Ӧ���ʣ�v��A��=2mol?L-1?s-1
�淴Ӧ���ʣ�v��B��=2mol?L-1?s-1
D������Ӧ���ʣ�v��A��=1mol?L-1?s-1
�淴Ӧ���ʣ�v��C��=1.5mol?L-1?s-1
4��ѡ���� ���ڷ�ӦN2(g)+3H2(g) 2NH3(g)?��H=��92kJ/mol����ֻ�ı�����һ��������һ������������Ӧ������ʹƽ��������Ӧ�����ƶ����ǣ�?��
2NH3(g)?��H=��92kJ/mol����ֻ�ı�����һ��������һ������������Ӧ������ʹƽ��������Ӧ�����ƶ����ǣ�?��
A�������¶�
B�������������
C������c(NH3)
D������������Ũ�Ⱦ�����ԭ����2��
5������� ��Ԫ�����ڱ��д�������λ�õ�Ԫ���ڽṹ�����������������Ƶĵط����ڶ����ڵ�̼�������������������γ��⻯���Ԫ�ص��⻯���H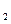 O�⣬����H
O�⣬����H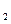 O
O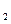 ��̼Ԫ�ص��⻯���CH
��̼Ԫ�ص��⻯���CH �⣬����C
�⣬����C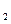 H
H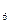 �ȣ���֮���Ƶĵ�Ԫ�ص��⻯����⣬����N
�ȣ���֮���Ƶĵ�Ԫ�ص��⻯����⣬����N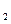 H
H �ȡ�
�ȡ�
��1��̼ԭ��֮����Խ�ϳ���״�ṹ����ԭ��֮��Ҳ�����γ���״�ṹ�����赪ԭ�Ӽ�ֻ�Ե���������ʽ���ӳ���״�����γ��⻯����ϵ���⻯���ͨʽΪ?��
��2����ϵ���е�N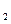 H
H �ǡ�����������ʱ������õ�Һ��ȼ�ϣ�Һ̬������������������������Һ̬ȼ�ϵ��ŵ��Dz�����������������Ⱦ����֪40g N
�ǡ�����������ʱ������õ�Һ��ȼ�ϣ�Һ̬������������������������Һ̬ȼ�ϵ��ŵ��Dz�����������������Ⱦ����֪40g N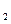 H
H �ڻ������ʱ��Ӧ�зų�710kJ������д���������ʱ�÷�Ӧ���Ȼ�ѧ����ʽ��??��
�ڻ������ʱ��Ӧ�зų�710kJ������д���������ʱ�÷�Ӧ���Ȼ�ѧ����ʽ��??��
��3����ϵ�����е�NH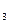 ��ũҵ����ѧ��������ҵ������Ҫ���塣��ϳ�ԭ��Ϊ��
��ũҵ����ѧ��������ҵ������Ҫ���塣��ϳ�ԭ��Ϊ��
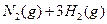 ?
? ?
?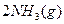 ?
?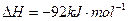
I����һ���¶��£���1.5molN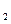 ��6 molH
��6 molH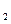 ͨ�뵽һ���̶��ݻ�ΪVL���ܱ������У�����Ӧ�ﵽƽ��ʱ�������������ѹǿΪ��ʼʱ��80%����
ͨ�뵽һ���̶��ݻ�ΪVL���ܱ������У�����Ӧ�ﵽƽ��ʱ�������������ѹǿΪ��ʼʱ��80%����
��ʱ��Ӧ�ų�������Ϊ??kJ.
H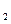 ��ת����=?��
��ת����=?��
���¶��ºϳɰ���Ӧ��ƽ�ⳣ��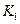 =?��ֻ�����ֱ���ʽ��
=?��ֻ�����ֱ���ʽ��
II���ڱ����¶Ȳ��䣬��ͬ������ܱ������У�����ʼ�����ʵ�����ΪamolN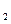 ��bmolH
��bmolH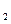 ��cmolNH
��cmolNH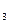 ,ƽ��ʱNH
,ƽ��ʱNH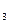 �����ʵ�������Ϊ25%����
�����ʵ�������Ϊ25%����
�ﵽƽ��ʱ��I��II�ų�������?������ĸ���ţ�
A��һ�����
B��ǰ��һ��С�ں���
C��ǰ�ߵ��ڻ�С�ں���
D��ǰ�ߵ��ڻ���ں���
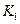 ��
��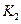 ��ͬ
��ͬ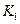 ?
?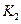 �������������
������������� ����
���� ��=����
��=����