微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol・L-1,则该溶液中溶质的pC=3。下列表达正确的是
A某温度下任何电解质的水溶液中,pC(H+) +pC(OH-)=14
B 0.01mol/L的CaCl2溶液中逐渐滴加纯碱溶液,滴加过程中pC(Ca2+)逐渐减小
C用0.01mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大
D.某温度下,AB难溶性离子化合物的Ksp=1.0×10-10, 其饱和溶液中pC(A+) +pC((B-)=10
参考答案:D
本题解析:pC(H+) +pC(OH-)=14,只是常温下成立,A错;CaCl2溶液中逐渐滴加纯碱溶液,C(Ca2+)减小,pC增大,B错;某浓度的NaOH溶液中滴加盐酸,OH?的物质的量浓度减少,而H+的物质的量浓度增大,即pC(H+)减少,C错。
本题难度:一般
2、选择题 已知下面三个数据:7.2×10-4、4.6×10-4、4.9 ×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:
NaCN+HNO2===HCN+NaNO2
NaCN+HF===HCN+NaF
NaNO2+HF===HNO2+NaF
由此可判断下列叙述不正确的是
[? ]
A.K(HF)=7.2 ×10-4
B.K(HNO2)=4.9 ×10-10
C.根据其中两个反应即可得出结论
D.K(HCN)<K(HNO2)<K(HF)
参考答案:B
本题解析:
本题难度:一般
3、选择题 相同温度、相同物质的量浓度的下列各组溶液,按pH值依次减小的顺序排列的是( )
A.CH3COONa、Na2CO3、NaHSO4、NaCl
B.HCl、CH3COOH、NH4Cl、NaHCO3
C.NaOH、Ba(OH)2、H2SO4、HCl
D.NH4Cl、CH3COOH、NaHSO4、H2SO4
参考答案:D
本题解析:
本题难度:一般
4、选择题 在0.10 mol・L-1CH3COOH溶液中存在如下电离平衡:CH3COOH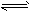 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
[? ]
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.10mol・L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
参考答案:B
本题解析:
本题难度:一般
5、选择题 某温度下HF的电离常数Ka=3.3×10-4 mol・L-1,CaF2的溶度积常数Ksp=1.46×10-10(mol・L-1)3。在该温度下取浓度为0.31 mol・L-1的HF与浓度为0.002 mol・L-1的CaCl2溶液等体积混合。下列说法正确的是(?)
A.该温度下,0.31 mol・L-1的HF溶液的pH=2
B.升高温度或增大浓度,HF的电离平衡常数都将增大
C.两溶液混合不会产生沉淀
D.向饱和的CaF2溶液中加水后,c(Ca2+)一定比加水前减小
参考答案:A
本题解析:A、电离常数Ka(HF)=3.3×10-4,HF为弱电解质,不能完全电离,25℃时,0.31mol/LHF溶液中c(H+)=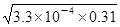 =1×10-2mol/L,pH=1,故A正确;B、电离常数只受温度的影响,不随浓度的变化而变化,故B错误;C、0.31 mol/L的HF溶液中c(H+)=c(F-)=1×10-2mol/L。故C错误;在该温度下取浓度为0.31 mol・L-1的HF与浓度为0.002 mol・L-1的CaCl2溶液等体积混合后c(F-)=0.5×10-2mol/L,c(Ca2+)=0.001mol/L,则c2(F-)×c(Ca2+)=(0.5×10-2)2×0.001=2.5×10-8>1.46×10-10,因此该体系中有CaF2沉淀产生,故C不正确。D、向饱和的CaF2溶液中加水后,溶液还可能是饱和的,所以c(Ca2+)不一定比加水前减小,D不正确,答案选A。
=1×10-2mol/L,pH=1,故A正确;B、电离常数只受温度的影响,不随浓度的变化而变化,故B错误;C、0.31 mol/L的HF溶液中c(H+)=c(F-)=1×10-2mol/L。故C错误;在该温度下取浓度为0.31 mol・L-1的HF与浓度为0.002 mol・L-1的CaCl2溶液等体积混合后c(F-)=0.5×10-2mol/L,c(Ca2+)=0.001mol/L,则c2(F-)×c(Ca2+)=(0.5×10-2)2×0.001=2.5×10-8>1.46×10-10,因此该体系中有CaF2沉淀产生,故C不正确。D、向饱和的CaF2溶液中加水后,溶液还可能是饱和的,所以c(Ca2+)不一定比加水前减小,D不正确,答案选A。
本题难度:一般