微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 为证明化学反应有一定的限度,进行如下探究活动:
I.取5mL 0.1mol/L的KI溶液,滴加5―6滴FeCl3稀溶液;?
Ⅱ.继续加入2mL CCl4,盖好玻璃塞,振荡静置。
Ⅲ.取少量分液后得到的上层清液,滴加KSCN溶液。
Ⅳ.移取25.00mLFeCl3稀溶液至锥形瓶中,加入KSCN溶液用作指示剂,再用c mol/LKI标准溶液滴定,达到滴定终点。重复滴定三次,平均耗用c mol/LKI标准溶液VmL。
(1)探究活动I中发生反应的离子方程式为?。
请将探究活动Ⅱ中“振荡静置”后得到下层液体的操作补充完整:将分液漏斗放在铁架台上,静置。
?。
(2)探究活动Ⅲ的意图是通过生成红色的溶液(假设溶质全部为Fe(SCN)3),验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈红色。对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+?猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察。
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,密度为0.71g/mL,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4―反应生成暗蓝色沉淀,用K4[Fe(CN)6](亚铁氰化钾)溶液检验Fe3+的灵敏度比用KSCN溶液更高。
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
实验操作
| 现象和结论
|
步骤一:
| 若产生暗蓝色沉淀,则?。
|
步骤二:
| 若乙醚层呈红色,则?。
|
?
②写出实验操作“步骤一”中的反应离子方程式:?。
(3)根据探究活动Ⅳ,FeCl3稀溶液物质的量浓度为?mol/L。
参考答案:(共14分)(1)2Fe3+ + 2I-=2Fe2+ + I2(2分);待液体分层后,将分液漏斗颈上的玻璃塞打开,或使玻璃塞上的凹槽(或小孔)对准分液漏斗上的小孔,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下。(2分)
(2)
实验操作
现象和结论
步骤一:取萃取后得到的上层清液,加入2滴K4[Fe(CN)6](亚铁氰化钾)溶液(2分)
若产生暗蓝色沉淀,则猜想一不成立(1分)
步骤二:取探究Ⅲ中所得溶液,加入少量乙醚,充分振荡,静置分层(2分)
若乙醚层呈红色,则猜想二成立(1分)
?
4Fe3+ +3[Fe(CN)6]4―=Fe4[Fe(CN)6]3↓(2分)?(3)0.04cV(2分)
本题解析:(1)铁离子具有氧化性,能把碘离子氧化生成单质碘,反应的离子方程式是2Fe3+ + 2I-=2Fe2+ + I2。探究活动Ⅱ是用四氯化碳萃取单质碘,因此正确的操作是将分液漏斗放在铁架台上,静置。待液体分层后,将分液漏斗颈上的玻璃塞打开,或使玻璃塞上的凹槽(或小孔)对准分液漏斗上的小孔,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下。
(2)①根据步骤1中实验现象是产生暗蓝色沉淀,这说明加入的试剂是K4[Fe(CN)6](亚铁氰化钾)溶液,所以步骤1是取萃取后得到的上层清液,加入2滴K4[Fe(CN)6](亚铁氰化钾)溶液。若产生暗蓝色沉淀,则猜想一不成立;根据步骤2中实验现象是乙醚层呈红色,这说明加入的试剂是乙醚,则步骤2的操作是取探究Ⅲ中所得溶液,加入少量乙醚,充分振荡,静置分层。若乙醚层呈红色,则猜想二成立。
②根据以上分析可知,实验操作“步骤一”中的反应离子方程式是4Fe3+ +3[Fe(CN)6]4―=Fe4[Fe(CN)6]3↓。
(3)根据方程式2Fe3+ + 2I-=2Fe2+ + I2可知
Fe3+~~~~~I-
1mol? 1mol
0.0250Lx? cmol/L×0.001VL
解得x=0.04cVmol/L
本题难度:困难
2、填空题 (6分) 在一定体积的密闭容器中,进行如下化学反
在一定体积的密闭容器中,进行如下化学反 应:
应:
CO2(g)+H2(g) CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
回答下列问题:
(1)该反应的化学平衡常数表达式为K=?。
(2)该反应为?反应(选填吸热、放热)。
参考答案:(1)略(2)吸热(3)bc
本题解析:略
本题难度:一般
3、选择题 可逆反应3H2+N2 2NH3达到平衡的标志是(? )。
2NH3达到平衡的标志是(? )。
①消耗3 mol H2的同时生成2 mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3∶1∶2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成
A.①②⑤
B.②④
C.①②③④
D.全部
参考答案:B
本题解析:①消耗3 mol H2的同时消耗2 mol NH3,②1个N≡N键断裂的同时,有3个H-H键形成④1个N≡N键断裂的同时,有6个N-H键断裂,平衡状态的标志。
本题难度:一般
4、选择题 可逆反应:3A(g)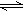 3B(?)+C(?)(△H>0),随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是(?)
3B(?)+C(?)(△H>0),随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是(?)
A.B和C可能都是固体
B.B和C只能有一个是气体
C.B和C一定都是气体
D.若C为固体,则B一定是气体
参考答案:D
本题解析:混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,由于正反应是吸热反应,所以升高温度,平衡向正反应方向移动,所以如果BC都是气体,则可能正确。如果BC都不是气体,则相对分子质量不变。如果C是固体,B是气体,也是正确的,因此正确的答案选D。
本题难度:一般
5、选择题 能用勒夏特列原理解释的是(?)?
A.红棕色的NO2,加压后颜色先变深后变浅
B.工业上合成NH3反应使用催化剂
C.实验室可以采用排饱和食盐水收集Cl2
D.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
参考答案:AC
本题解析:在其它条件不变时,改变影响平衡的一个条件,平衡就向能减弱这种改变的方向进行,这就是勒夏特列原理。在NO2中存在平衡2NO2 N2O4,增大压强平衡向正反应方向移动,所以A正确。催化剂不能改变平衡状态,不能用勒夏特列原理解释。饱和食盐水中氯离子的浓度大,能抑制氯气的溶解,正确。D中的可逆反应是反应前后体积不变的,所以改变压强,平衡不移动,不能用勒夏特列原理解释。答案是AC。
N2O4,增大压强平衡向正反应方向移动,所以A正确。催化剂不能改变平衡状态,不能用勒夏特列原理解释。饱和食盐水中氯离子的浓度大,能抑制氯气的溶解,正确。D中的可逆反应是反应前后体积不变的,所以改变压强,平衡不移动,不能用勒夏特列原理解释。答案是AC。
本题难度:简单