微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)
含硫化合物在工业生产中有广泛的用途。
(1)对于可逆反应2SO2(g)+O2(g)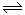 2SO3(g) △H<0,下列研究目的和图示相符的是?
2SO3(g) △H<0,下列研究目的和图示相符的是?
(填序号)
序号
| A
| B
| C
| D
|
目的
| 压强对平衡的影响
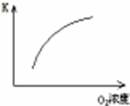
| 温度对转化率的影响
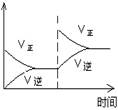
| 增加O2浓度对速率的影响
| 浓度对平衡常数的影响
|
图示
| 
| 
| 
| 
|
(2)在5000C有催化剂存在的条件下,向容积为2L的甲乙两个密闭容器中均充入2molSO2和1molO2。甲保持容积不变,乙保持压强不变,充分反应后,均达平衡状态,此时SO3的体积 91exam.org分数甲
?乙。(填“>”“<”或“="”" )
(3)向2L的甲容器中充入2molSO2、1molO2,测得SO2的平衡转化率与温度的关系如下图所示。
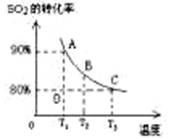
Ⅰ.在T1温度下,反应进行到状态D时,v正?v逆。(填“>”“<”或“="”" )
Ⅱ.T3温度下,平衡时测得反应放出的热量为Q1,在相同温度下若再向容器中通入2molSO2、1molO2,重新达到平衡,测得反应又放出热量Q2 。则下列说法中正确的是?。(填序号)
A.相同温度下新平衡时容器中的压强是原平衡时的两倍
B.Q2一定大于Q1
C.新平衡时SO2的转化率一定大于80%
(4)在甲容器中充入一定量的SO2和1.100molO2,在催化剂作用下加热,当气体的物质的量减少0.315mol时反应达到平衡,此时测得气体压强为反应前的82.5%,则SO2的转化率为?。
(5)若用氢氧化钠溶液吸收SO2气体恰好得到酸式盐,已知该酸式盐溶液呈弱酸性,则溶液中各离子浓度由大到小的顺序为?。(用离子浓度符号表示)
(6)一定温度下,用水吸收SO2气体,若得到pH=5的H2SO3溶液,则溶液中亚硫酸氢根离子和亚硫酸根离子的物质的量浓度之比为? ?。(已知该温度下H2SO3的电离常数:Ka1=1.0×10-2mol/L,Ka2=6.0×10-3mol/L)
2、选择题 可逆反应A(g)+B C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是(?)
C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是(?)
A.增大A的浓度,平衡体系颜色加深,则说明D是有颜色的气体
B.若升高温度,C的百分含量减少,则说明正反应为放热反应
C.若增大压强,平衡不移动,则说明B和D一定都是气体
D.如果B是气体,则增大A的浓度会使B的转化率增大,A的转化率减少
3、填空题 将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:
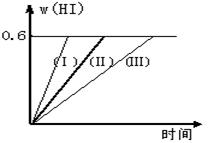
I2(g) + H2(g)  ?2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
?2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
(1)达平衡时,I2(g)的物质的量浓度为?写出该反应的平衡常数表达式? _____________________________________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是?,则乙条件可能是??。
(填入下列条件的序号)
①恒容条件下,升高温度;? ②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积;? ④恒温条件下,扩大反应容器体积;? ⑤恒温恒容条件下,加入适当催化剂。
4、选择题 在一定条件下,某容器中充入N2和H2合成NH3,以下叙述中错误的是 :?
A.开始反应时,正反应速率最大
B.随着反应的进行,正反应速率逐渐减小,最后正反应速率减小为零
C.随着反应的进行,逆反应速率逐渐增大,最后保持恒定
D.随着反应的进行,正反应速率逐渐减小,最后与逆反应速率相等且都保持恒定
5、选择题 将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应: H2NCOONH4(s) 2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
?
| 平衡浓度/ (mol L-1)
|
c(NH3)
| c(CO2)
|
T1
| 0.1
| ?
|
T2
| ?
| 0.1
|
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的物质的量:Δn(T2)=2Δn(T1)